e-ISSN: 2215-3896.
(Julio-Diciembre, 2021). Vol 55(2)
DOI: https://doi.org/10.15359/rca.55-2.15
Open Acces: www.revistas.una.ac.cr/ambientales
e-Mail: revista.ambientales@una.cr
Licencia: CC BY NC SA 4.0
NOTA TÉCNICA
Calidad de plántulas de Swietenia mahagoni L. Jacq. producida en sustratos inoculados con hongo micorrízico arbuscular
Plant quality of Swietenia mahagoni L. Jacq. produced in substrate inoculated with arbuscular mycorrhizal fungi
Emir Falcón Oconor1, Milagros Cobas López2, Marta Bonilla Vichot3, Orfelina Rodríguez Leyva4, Caridad Virgen Romero Castillo5, Eliabin Rodríguez Leyva6
[Recibido: 27 de mayo 2020, Aceptado: 28 de enero 2021, Corregido: 17 de febrero 2021, Publicado: 1 de julio 2021]
Resumen
[Introducción]: La asociación micorrícica es una estrategia nutricional desarrollada por algunas plantas y hongos que les asegura un beneficio mutuo. [Objetivo]: Evaluar el efecto de la utilización de cepas de hongos micorrízicos arbusculares (HMA) en el crecimiento y calidad de la planta Swietenia mahagoni L. Jacq. cultivadas en sustratos orgánicos. [Metodología]: El experimento se desarrolló en el vivero del Centro de Estudio de Tecnología Agroforestal, Universidad de Guantánamo (UG), entre enero y abril de 2019. Con un diseño completamente al azar, se evaluaron las combinaciones de dos factores: sustratos (cascarilla de cacao + fibra de coco + aserrín de pino compostados en proporción 6:2:2 y 2:6:2) y cepas de HMA (Glomus cubense, Rhizophagus intraradices, Funneliformis mosseae y sin inoculación). Se evaluó la altura, el diámetro del cuello de la raíz, el área foliar, la masa seca de la parte aérea y radical, esbeltez, índice de Dickson, colonización micorrízica y el índice de calidad de la planta. [Resultados]: Se encontraron interacciones significativas (p ≤ 0,001) entre los factores para todas las variables evaluadas. Existió un efecto diferenciado de las micorrizas en el crecimiento de la caoba antillana. Las cepas de micorrizas Glomus cubense, Rhizophagus intraradices y Funneliformis mosseae, en el sustrato dos (60 % fibra de coco), propiciaron incrementos significativos en el crecimiento y calidad de la planta. [Conclusiones]: Es evidente la importancia de la asociación micorrízica para obtener plántulas de Swietenia mahagoni de alta calidad para el establecimiento de plantaciones.
Palabras clave: Biofertilizante; micorriza; plántula; vivero.
Abstract
[Introduction]: The mycorrhizal association is a nutritional strategy that some plants and mushrooms have developed that assures them a mutual benefit. [Objective]: To evaluate the effect of the use of arbuscular mycorrhizal fungi strains (AMF) in the growth and quality of Swietenia mahagoni L. Jacq. seedlings, produced with organic substrates. [Methodology]: It was carried out an investigation at the Forestry Technology Study Center of Guantánamo University from January to April 2019. A complete random block design was utilized to study the combinations of two factors: two substrates (cocoa husk + coconut fiber + pine sawdust in proportions 6:2:2 and 2:6:2) and AMF strains (Glomus cubense, Rhizophagus intraradices, Funneliformis mosseae and without inoculation). Seedling total height, stem diameter, leaf area, aerial and root dry biomass, height/diameter ratio, Dickson Index, mycorrhizal colonization and a quality index were utilized as response variables. [Results]: Significant interactions for all variables studied were determined (p ≤ 0,001) among the studied factors. There was a differentiate effect of the mycorrhizal in the growth of Antillean mahogany seedlings. The mycorrhizal strains Glomus cubense, Rhizophagus intraradices and Funneliformis mosseae, in the second substrate (60 % coconut fiber) promoted a significant growth increment, as well as a major seedling quality. [Conclusions]: It is evident the effect of the mycorrhizal association in the production and quality of Swietenia mahagoni seedlings for the establishment of plantations.
Keywords: Biofertilizers; mycorrhiza; nursery; seedling.
Probablemente, Swietenia mahagoni L. Jacq. es una de las especies maderables más valiosas del mundo, la más conocida y apreciable para ebanistería y toda clase de obra que requiera madera de alta calidad; que ha sido exportada a Europa y Estados Unidos por más de cuatro siglos. Pertenece a la familia Meliaceae y es conocida en Cuba con los nombres comunes de caoba, caoba antillana o caoba de Cuba (Betancourt, 1999).
Las investigaciones en Cuba sobre S. mahagoni se han enfocado en el estudio de sus características morfológico-funcionales, ecológicas y propagación in vitro (Ricardo, Puentes, y Torres, 2016; Barbón et al., 2013), pero muy pocas han tenido como objetivo el estudio de las relaciones simbióticas que establece con microorganismos del suelo, lo que mejora el crecimiento y calidad de la planta en vivero. Los resultados de estos estudios pueden contribuir a mejorar la productividad de las plantaciones forestales (Oros et al., 2015).
La efectividad de la micorriza, pues, depende de factores físicos y químicos (pH, fósforo y nitrógeno, entre otros) ofrecidos por el sustrato, que determinan qué tan favorable es la simbiosis entre plantas y hongos, y cuánto mejor será el desarrollo de las especies vegetales (Li et al., 2016).
Producir plantas de calidad en vivero contribuye a garantizar mayor porcentaje de supervivencia en las plantaciones forestales y en los programas de reforestación (Rueda et al., 2014). El desarrollo de protocolos y estrategias para la producción de plántulas con calidad, en menor tiempo y en condiciones asequible es muy importante. De esta manera, estudios que relacionan sustratos alternativos y la inoculación de las plántulas con hongos micorrízicos arbusculares, así como microorganismos que favorecen o estabelecimiento de las plántulas en las áreas degradadas (Feijen et al., 2018), son de grande valía. El efecto de la interacción sustrato-micorrízica puede contribuir a obtener plántulas con mejor calidad en vivero y alta supervivencia al trasplantar a campo. El presente estudio evalúa el efecto de dichos factores en el crecimiento y calidad de S. mahagoni en fase de vivero.
Se utilizaron plántulas de S. mahagoni producida en vivero bajo umbráculo de malla verde con 50 % de sombra ubicado en Centro de Estudio de Tecnología Agroforestal (CETAF) perteneciente a la Universidad de Guantánamo, localizado en las coordenadas geográficas 20°12´21´´ de latitud norte y los 75°13´37´´ de longitud oeste a 87 m s.n.m. Respectivamente, según información del Instituto de Meteorología de Cuba (INSMET, 2019), el clima presenta una marcada estacionalidad seca de noviembre a marzo; y lluvias desde abril hasta junio y septiembre hasta octubre. Este sitio posee una precipitación y temperatura media anual de 1 028 mm y 25.9 °C.
Según la Norma Cubana NC: 71-04/87, las semillas de S. mahagoni se obtuvieron de la nave semillera de la Empresa Agroforestal Guantánamo, certificadas en el Instituto de Investigaciones Agroforestales de Baracoa.
El experimento siguió un diseño experimental completamente al azar, con arreglo factorial para evaluar los factores sustrato y microorganismos (2x4 respectivamente) (Cuadro 1). Se utilizaron 5 réplicas por cada uno de los 8 tratamientos, con 10 plántulas cada una (50 individuos por tratamiento).
Cuadro 1. Descripción de los tratamientos aplicados en el experimento.
Table 1. Treatments description, applied in the experiment.
|
Tratamientos |
Código |
Cepas de HMA |
Sustratos |
|
1 |
M0/S1 |
No |
S1 |
|
2 |
M0/S2 |
No |
S2 |
|
3 |
M1/S1 |
Glomus cubense |
S1 |
|
4 |
M1/S2 |
Glomus cubense |
S2 |
|
5 |
M2/S1 |
Rhizoglomus intraradices |
S1 |
|
6 |
M2/S2 |
Rhizoglomus intraradices |
S2 |
|
7 |
M3/S1 |
Funneliformis mosseae |
S1 |
|
8 |
M3/S2 |
Funneliformis mosseae |
S2 |
S1= Cascarilla de cacao + Fibra de coco + Aserrín de pino en proporción 6:2:2; S2= Cascarilla de cacao + Fibra de coco + Aserrín de pino compostados en proporción 2:6:2; HMA= Hongo Micorrízico Arbuscular.
La mezcla de compuestos orgánicos utilizado como sustrato (Cascarilla de cacao-Fibra de coco-Aserrín de pino compostados) para la producción de las plántulas de Caoba antillana fue escogida en función de los buenos resultados obtenidos por Falcón et al. (2019). La mezcla fue tamizada por una malla de 4 mm y esterilizada en autoclave a 121 ºC a 1 atm de presión por 120 minutos.
En el momento de la siembra en tubetes de 200 cm3, las semillas se inocularon por el método de recubrimiento (Fernández et al., 2001) con las cepas de inóculos micorrízicos certificados: INCAM-2: Funneliformis mosseae (Schüßler y Walker, 2011); INCAM 4: Glomus cubense (Rodríguez et al., 2011) e INCAM-11: Rhizoglomus intraradices (Schüßler y Walker, 2011) con una calidad mínima garantizada de 20 esporas g-1 de inoculante, producto no tóxico y libre de patógenos, procedentes del cepario del Instituto Nacional de Ciencias Agrícolas (INCA).
Las características químicas-físicas del sustrato y sus intervalos óptimos sugeridos por Abad et al., (2005) y Arévalo et al., (2016), se presentan en el Cuadro 2, los que se encuentran entre los valores óptimos, no así para el sustrato dos en el que el fosforo se encuentra por debajo del intervalo óptimo.
Cuadro 2. Caracterización química-física de los sustratos.
Table 2. Chemistry-physical characterization of the substrate.
|
Sustrato |
Propiedades químicas |
||||||||
|
pH |
MO (%) |
N (%) |
P (%) |
K+ (%) |
CE (dS.m-1) |
||||
|
S1 |
6.20 |
77.20 |
1.86 |
1.43 |
1.79 |
3.13 |
|||
|
S2 |
7.70 |
66.66 |
1.40 |
0.10 |
1.19 |
2.27 |
|||
|
Valores óptimos |
5.3-6.5 |
>50 |
>1.3 |
>0.7 |
>0.2 |
<3.5 |
|||
|
Sustrato |
Propiedades físicas |
||||||||
|
DA (g mL-1) |
DR (g mL-1) |
PT (%) |
DMP (mm) |
RH (%) |
|||||
|
S1 |
0.38 |
1.67 |
82.02 |
0.45 |
65.49 |
||||
|
S2 |
0.31 |
1.68 |
76.16 |
0.35 |
70.76 |
||||
|
Valores óptimos |
0.2-0.4 |
1.45-2.64 |
75-85 |
- |
>50 |
||||
2.1 Caracterización de la planta en vivero
Al cabo de los 55 días de germinación, se comenzó la medición de los parámetros morfológicos; la altura se midió con una regla graduada en centímetros, desde la base del tallo hasta la yema apical y el diámetro se registró en milímetros en la base del tallo, con un pie de rey,
Al final del experimento (120 días), se evaluó el área foliar utilizando un medidor de área foliar Portable Area Meter Model LI-3000A (LI-COR®) y la biomasa seca total de la planta, para lo cual se colectaron todas las partes de las plantas, se empacaron en bolsas de papel y fueron llevadas a estufa (Binder®) a una temperatura constante de 60 ºC por 72 h. Luego se determinó el peso seco aéreo (PSA), radical (PSR) y total (PST). Con los datos obtenidos se calcularon los siguientes índices morfológicos obtenidos de Rueda et al., (2014):
-Esbeltez (H/DCR): es el cociente de la altura en cm dividido por el diámetro en mm.
-Relación parte aérea/parte radical (PSA/PSR): se estimó como el cociente entre el peso seco de la parte aérea y el peso seco de la raíz en gramos.
-Índice de calidad de Dickson (ICD): el ICD se determinó mediante la Ecuación 1:
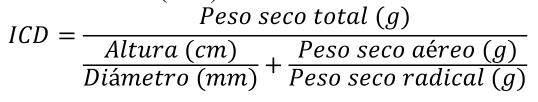 (E.1)
(E.1)
-Calidad de la planta (CP): la CP se determinó mediante la Ecuación 2 citada por Panduro (2017):
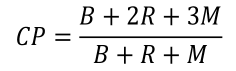 (E.2)
(E.2)
Donde:
B= Individuos en condiciones buenas para plantas de tallo limpio sin defectos o enfermedades;
R= Individuos en condiciones regulares para plantas atacadas por enfermedades o con defectos y
M= Individuos en condiciones malas para plantas muertas.
La calidad de la planta se evalúa mediante el coeficiente de calidad según escala de valores citado por Panduro (2017), que se presenta en la Cuadro 3:
Cuadro 3. Coeficiente de calidad.
Table 3. Coefficient of quality.
|
Calidad de planta |
Valor (coeficiente) |
|
Excelente (E) |
1.0 a < 1.1 |
|
Buena (B) |
1.1 a < 1.5 |
|
Regular (R) |
1.5 a < 2.2 |
|
Mala (M) |
2.2 a 3.0 |
A las variables evaluadas en cada uno de los tratamientos se les analizó la homocedasticidad y normalidad de los datos, utilizando, respectivamente, los criterios de Levene y Kolmogorov-Smirnov. Posteriormente, se sometieron a análisis de varianza (Anova) y las medias se compararon con la prueba de Duncan (p < 0.05). Al parámetro calidad de la planta se les realizó una prueba chi-cuadrado (X2) mediante un análisis de contingencia (p < 0.05). Todos los análisis se realizaron con el programa estadístico SPSS ver. 23 para Windows.
El Cuadro 4 presenta el análisis de varianza, este mostró efectos significativos (p≤ 0.001) para todos los parámetros e índices morfológicos evaluados. La interacción entre los factores sustratos y cepas de HMA utilizados fue altamente significativa (p≤ 0.001) en todos los parámetros evaluados.
Cuadro 4. Análisis de varianza para los parámetros e índices morfológicos de la planta S. mahagoni a los cuatro meses de cultivada.
Table 4. Variance analysis for the parameters and morphological indexes of the plant S. mahagoni to the four months of cultivated.
|
Factor de variación |
G.L |
Cuadrados medios y significancia (P) |
||||
|
Altura (cm) |
Diámetro (mm) |
Esbeltez |
Índice de Dickson |
Área foliar (cm2) |
||
|
Sustrato (S) |
1 |
41.60*** |
3.05** |
0.05* |
0,004* |
5,99* |
|
Cepas (HMA) |
3 |
131.87*** |
11.27** |
0.18* |
0.05*** |
67.49*** |
|
S X HMA |
3 |
29.18*** |
2.70** |
0.19** |
0.01** |
3.09*** |
|
Factor de variación |
G.L |
Cuadrados medios y significancia (P) |
||||
|
Peso seco aéreo (g) |
Peso seco radical (g) |
Colonización micorrízica (%) |
Relación peso seco aéreo/peso seco radical |
|||
|
Sustrato (S) |
1 |
0.01* |
0,02* |
143.93*** |
0.02* |
|
|
Cepas (HMA) |
3 |
0.19*** |
0.31*** |
11293.90*** |
0.49*** |
|
|
S X HMA |
3 |
0.01* |
0.02* |
27.319*** |
0.06* |
|
*= P < 0.05; **= P < 0.01; ***= P < 0.001; G.L= Grado de libertad.
En los parámetros altura, diámetro del cuello de la raíz, esbeltez e índice de Dickson (Cuadro 5), se observó que las plántulas desarrolladas en el sustrato S2 inoculado con las cepas G. cubense y R. intraradices (M1/S2 y M2/S2) fueron las que alcanzaron los mayores valores, difiriendo estadísticamente con el resto de los tratamientos. Los tratamientos no inoculados (M0/S1 y M0/S2) fueron los que presentaron los menores valores. Esto puede estar relacionado con los beneficios proporcionados por la micorriza en el crecimiento de las plantas.
Cuadro 5. Comportamiento de parámetros de crecimiento e índices morfológicos de S. mahagoni a los cuatro meses de cultivada.
Table 5. Growth parameters response and morphological indexes of S. mahagoni at four months cultivated.
|
Tratamientos |
Altura (cm) |
Diámetro del cuello de la raíz (mm) |
Esbeltez (H/Dcr) |
Índice de calidad de Dickson (ICD) |
|
|
1 |
M0/S1 |
19.34e |
3.97d |
4.89a |
0.16c |
|
2 |
M0/S2 |
17.31f |
3.52d |
4.97a |
0.14c |
|
3 |
M1/S1 |
26.29b |
6.25c |
4.23b |
0.26b |
|
4 |
M1/S2 |
29.75a |
7.90a |
3.78d |
0.31a |
|
5 |
M2/S1 |
24.61d |
6.38b |
3.86c |
0.27b |
|
6 |
M2/S2 |
28.20b |
7.56a |
3.75d |
0.30a |
|
7 |
M3/S1 |
24.18d |
6.20c |
3.90bc |
0.24b |
|
8 |
M3/S2 |
25.10c |
6.67b |
3.76d |
0.25b |
|
ES* |
0.465* |
0.169* |
0.067* |
0.006* |
|
Medias con letras desiguales difieren estadísticamente según dócima de Duncan para p < 0.05. *Error estándar
Relacionado con el peso seco, colonización micorrízica y área foliar (Cuadro 6), se puede observar diferencia significativa entre tratamientos. Por eso, se ven favorecidas las plántulas desarrolladas en los sustratos micorrizados. No obstante, las plántulas desarrolladas en el sustrato S2 inoculado con las cepas G. cubense y R. intraradices (M1/S2 y M2/S2) alcanzaron los mayores valores, difiriendo estadísticamente con el resto de los tratamientos, en la relación peso seco aéreo/peso seco radical, colonización micorrízica y área foliar.
Cuadro 6. Efecto de los tratamientos en el peso seco, colonización micorrízica y el área foliar de la planta S. mahagoni a los cuatro meses de cultivada.
Table 6. Effect of the treatments in the dry weight, colonization mycorrhiza and the leaf area the plant S. mahagoni to the four months of cultivated.
|
Tratamientos |
Peso seco (g) |
Relación Peso seco aéreo/Peso seco radical (g) |
Colonización micorrízica (%) |
Área foliar (cm2) |
||
|
Aéreo |
Radical |
|||||
|
1 |
M0/S1 |
0.63d |
0.42e |
1.50a |
- |
9.55c |
|
2 |
M0/S2 |
0.58d |
0.35e |
1.67a |
- |
9.15c |
|
3 |
M1/S1 |
0.76b |
0.53d |
1.44b |
48.25b |
12.45b |
|
4 |
M1/S2 |
0.84a |
0.68a |
1.26d |
52.45a |
13.85a |
|
5 |
M2/S1 |
0.76b |
0.62bc |
1.31c |
46.31c |
12.85b |
|
6 |
M2/S2 |
0.81ab |
0.65ab |
1.26d |
51.35a |
13.78a |
|
7 |
M3/S1 |
0.75b |
0.57cd |
1.35b |
40.75c |
12.10b |
|
8 |
M3/S2 |
0.74bc |
0.56cd |
1.30c |
42.25c |
12.35b |
|
ES* |
0.011* |
0.015* |
0.024* |
0.026* |
0.035* |
|
Medias con letras desiguales difieren estadísticamente según dócima de Duncan para p < 0.05. *Error estándar.
En la mayoría de los tratamientos, la calidad de la planta (Figura 1) resultó buena, excepto en M0/S1 y M0/S2 donde se aprecian plántulas con características de inferior calidad en todos los parámetros evaluados, que las clasifica como mala. A través del coeficiente de contingencia de 0.799, se corrobora interacción entre los factores (sustratos x microorganismos) con diferencias significativas en la calidad de las plantas (p < 0,05), como efecto de los tratamientos investigados, por lo que hay evidencia de que la inoculación del sustrato con hongos micorrizógenos incide favorablemente en la calidad de la planta.
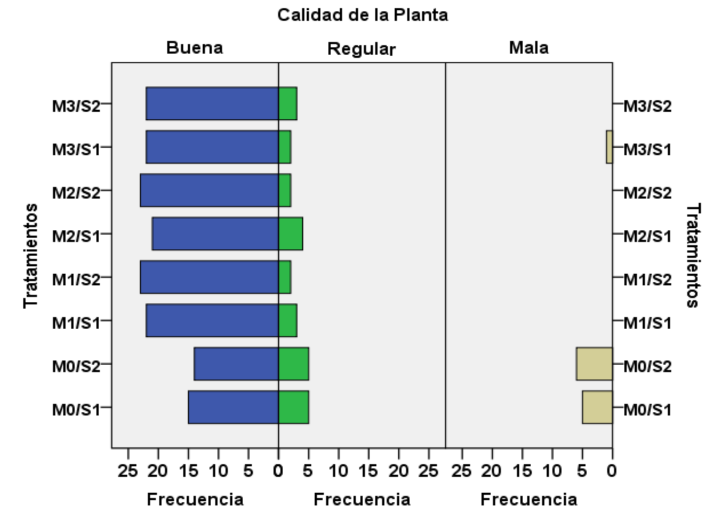
Figura 1. Histograma de frecuencia con los niveles de calidad de la planta.
Figure 1. Histogram of frequency with the levels of the plant quality.
Con respecto al valor del coeficiente de calidad citado por Panduro (2017), las plántulas son categorizadas de excelente en el sustrato S2 inoculado con las cepas G. cubense y R. intraradices (M1/S2 y M2/S2) y buena en el restante de los tratamientos donde el sustrato fue inoculado, no así para los tratamientos no inoculado (M0/S1 y M0/S2) las que son evaluadas como regular (Cuadro 7).
Cuadro 7. Efecto de los sustratos y microorganismos en la calidad de la planta de S. mahagoni a los cuatro meses de cultivada.
Table 7. Effect of the substrate and microorganism in the plant quality of S. mahagoni to the four months of cultivated.
|
Tratamientos |
Calificación de la calidad de la planta (CP) |
||
|
Coeficiente |
Interpretación |
||
|
1 |
M0/S1 |
1.60 |
Regular |
|
2 |
M0/S2 |
1.68 |
Regular |
|
3 |
M1/S1 |
1.12 |
Buena |
|
4 |
M1/S2 |
1.08 |
Excelente |
|
5 |
M2/S1 |
1.16 |
Buena |
|
6 |
M2/S2 |
1.08 |
Excelente |
|
7 |
M3/S1 |
1.16 |
Buena |
|
8 |
M3/S2 |
1.12 |
Buena |
Los resultados del presente estudio muestran que la inoculación con Hongos Micorrízicos Arbusculares tiene un efecto positivo en el crecimiento y calidad de la planta de S. mahagoni en condiciones de vivero. Con la inoculación de las cepas Glomus cubense y Rhizoglomus intraradices se evidencia mayor crecimiento, esto provoca un efecto sinérgico cuando el sustrato fue inoculado con las distintas cepas micorrízicas, fundamentalmente en los tratamientos donde se utiliza el sustrato S2 (M1/S2, M2/S2 y M3/S2). Esto permitió que las plántulas de caoba antillana crecieran en promedio 7.7 cm más en comparación con los tratamientos donde no se aplicó micorriza.
Este comportamiento pudiera estar relacionado con la disminución del contenido de fósforo disponible en el sustrato S2. Al respecto, para Rodríguez (2010) la actividad y el beneficio de la simbiosis es más visible en suelos deficientes en fósforo. En esta condición, plantas de Swietenia macrophylla inoculadas con hongos micorrízicos arbusculares (HMA) presentaron mayores tasas de crecimiento. La aplicación de fósforo influye considerablemente sobre el desarrollo de las micorrizas. Se ha reportado que pequeñas aplicaciones a los suelos, tanto inoculados como esterilizados, incrementaron el porcentaje de colonización, sin embargo, se reporta un efecto contrario con altas adiciones de este elemento (Bustamante y Rojas, 2017). Esta situación podría explicar el comportamiento de las cepas estudiadas en este experimento, pues el sustrato uno (S1) se caracterizó por valores superiores de fósforo disponible.
Por otra parte, el mayor porcentaje de fibra de coco (60 %) en el sustrato S2, favoreció el crecimiento, lo que coincide con Klein (2015), quien describe un buen desarrollo de las plantas cuando es utilizada la fibra de coco como componente en el sustrato. Los resultados favorables pueden explicarse a partir del análisis físico-químico del S2, donde se observa una baja DA y DMP pequeña. Lo que hace que el sustrato retenga alta cantidad de agua, ya que una cantidad adecuada de agua disponible es esencial para mantener la productividad de las plantas. La presencia de micorrizas puede influir de manera importante para regular la disponibilidad de agua e incrementar la biomasa, sobre todo en la parte radicular (Gómez et al., 2013).
En cuanto al índice de esbeltez (H/Drc), un valor inferior a 6 se considera adecuado para plantas latifoliadas (Rueda et al., 2014). En el presente estudio los valores fueron inferiores para todos los tratamientos, donde se alcanzaron los mejores índices de H/Drc, en los tratamientos donde el sustrato fue inoculado con las cepas micorrízicas. Fundamentalmente en los tratamientos (M1/S2, M2/S2 y M3/S2), de donde se infiere que serán plantas que podrían presentar una mayor resistencia mecánica a los fuertes vientos, asociado a una mejor calidad, plantas más esbeltas y con tallos vigorosos (Santin et al., 2018).
Al analizar los valores de ICD se pudo apreciar que los sustratos inoculados presentaron índices adecuados (0.24 y 0.31) para definir una planta de buena calidad. Dickson et al., (1960), consideran que cuanto más alto es el valor ICD, mejor es la calidad de la planta. En este sentido, los mayores valores fueron obtenidos en el sustrato S2 inoculado con las cepas G. cubense y R. intraradices (M1/S2 y M2/S2), que registraron índices adecuados (0.30 y 0.31) para definir una planta de buena calidad. Cabe destacar que en la mayoría de los trabajos donde se evalúa la calidad de las plantas en vivero, se trabaja bajo programas de fertirriego, donde las plantas están por periodos prolongados (8-12 meses) expuestas a condiciones ideales. Para el presente estudio se trabajó con la aplicación de micorriza arbuscular sin ningún apoyo de fertilizantes, solamente riego con agua a capacidad de campo. Por ello, los resultados de crecimiento de las plántulas de S. mahagoni obtenidos con los tratamientos M1/S2 y M2/S2, resultan promisorios y deberían conducir a disminuir la aplicación de fertilizantes comerciales en viveros forestales, para dar paso a la utilización de inóculos biológicos como biofertilizantes.
El crecimiento también fue favorecido, en biomasa aérea y radical, lo que representaría una mayor productividad. El efecto benéfico, además, se observó en la relación Peso seco aéreo/Peso seco radical, parámetro muy importante para el establecimiento de las plantas en campo. A menor valor de esta relación se ve favorecida la capacidad de absorción de agua. Esto es una condición favorable para la plantación en sitios marginales (Rueda et al., 2014), como las de la región de estudio. El mismo autor asevera que mientras menor valor se obtenga en esta relación para especies tropicales, existirá más vigor en la planta. En general, recomienda que, en sitios con precipitación escasa, el cociente no debe superar el valor de 2.5. En este sentido, los mejores valores fueron obtenidos en el sustrato S2 inoculado con las cepas G. cubense y R. intraradices (M1/S2 y M2/S2). El uso de hongos endomicorrizógenos en especies del género Swietenia cultivadas en vivero y destinadas a repoblaciones, se ha reportado en Swietenia macrophylla con resultados satisfactorios (Bango et al., 2013), así como en Swietenia mahagoni (Falcón et al., 2013) y en Swietenia humillis (Acosta, 2019).
Según lo revisado por Feijen et al. (2018), en las plantas con micotrófia facultativa se ve favorecida la colonización radical en condiciones de baja disponibilidad de nutrientes. Para diferentes estudios plantas que crecen en bajas condiciones de fósforo incrementan exudación de aminoácidos, estos reducen los azúcares y ácidos carboxílicos (Jones, Hodge y Kuzyakov, 2004), lo que favorece a la micorrización. Por esta razón, los mayores porcentajes de micorrización en el sustrato S2 inoculados con G. cubense y R. intraradices respectivamente con valores de 52.45 y 51.55 %,. Estos grados de micorrización fueron significativamente superiores a los alcanzados con F. mosseae en ambos sustratos (40.75 y 42.25 %). En todos los sustratos inoculados se presentaron porcentajes de micorrización entre 40.75 y 52.45 %. Estos resultados muestran la especificidad infectiva que establecen los HMA en las plantas, dependiendo de las características de cada sustrato (Feijin et al., 2018).
Los valores más altos asociados al área foliar se encontraron en los tratamientos M1/S2 y M2/S2, estadísticamente significativos al hacer su comparación con los tratamientos sin inoculación micorrízica. La mayor área foliar y biomasa se determinó con la utilización de las cepas micorrízicas G. cubense y R. intraradices. Lo cual indica que la especie caoba antillana, en la etapa de vivero, responde a la adición de estas cepas. Donde además se obtuvo mejores resultados cuando se usó el sustrato dos (S2). El uso de HMA presenta un efecto positivo en el crecimiento de las plantas, debido a los beneficios de esta simbiosis micorrízica, la que está relacionada con la nutrición vegetal (Smith y Smith, 2011). Por su parte, el sustrato dos, al presentar mayor porcentaje de fibra de coco (60 %), aporta nutrientes como calcio, nitrógeno y potasio. Lo que contribuye a mejorar la composición base de este sustrato, además de lograr una nutrición más balanceada (Falcón et al., 2019). Arévalo, Oberpaur y Méndez (2016), indican que la fibra de coco presenta ventajas de estabilidad física, porosidad total elevada (64.1 a 98.3 %), baja densidad aparente, (0.03 a 0.9 g cm-3) y una adecuada aireación (24.2 a 89.4 %).
La inoculación con HMA en el sustrato produce mejor calidad de plántula de S. mahagoni. La simbiosis planta-hongo se caracteriza por la presencia de estructuras fúngicas dentro y fuera de las raíces, que se extienden por el suelo como una red interconectada que funciona de interface entre el suelo y la planta. Con lo que aumenta la superficie de contacto de las raíces en el suelo y mejora la absorción de agua y nutrientes (Li et al., 2016).
Según resultados antes expuestos, los tratamientos M1/S2 y M2/S2 pueden utilizarse indistintamente. Esta opción posibilita la obtención de plántulas de mayor calidad, lo que valida la aptitud de estas combinaciones para ser utilizada en la producción de caoba antillana en condiciones similares a la del experimento. De igual manera, se reafirmó que F. mosseae como una segunda opción mostró valores por debajo de las otras cepas utilizadas en ambos tipos de sustratos, independientemente de su fertilidad. Bustamante y Rojas (2017), consignaron resultados semejantes con la inoculación de micorriza arbuscular en Theobroma cacao L.
El estímulo en el crecimiento, atribuible a la inoculación con hongos endomicorrízicos, ha sido reportado para algunas especies de la familia Meliaceae. Bango et al., (2013), registraron aumento en la altura, peso seco de raíz y diámetro de plantas de Swietenia macrophylla inoculadas con cepas micorrízicas del género Glomus. A su vez, Oros et al., (2015) demostraron que Cedrela odorata incrementó la biomasa aérea y radical cuando se inoculó con Rhizophagus intraradices. De igual forma Falcón et al., (2013) y Falcón et al., (2018), registraron mayor crecimiento y supervivencia en plántulas de Swietenia mahagoni L. Jacq., inoculadas con Rhizophagus intraradices y Glomus cubense, respectivamente, en comparación con las plantas sin inocular.
El sinergismo registrado debido a la inoculación de hongos endomicorrízicos y sustratos orgánicos, también se ha reportado previamente. Por ejemplo, Souza et al., (2009) reportaron el incremento de biomasa en la raíz de Schinus terebinthifolius en sustrato orgánico y esporas de las especies Gigaspora margarita y Glomus clarum. Acosta (2019) demostró que la inoculación con las cepas Glomus sp. y Acaulospora sp. en sustrato de origen industrial, incrementó el crecimiento y la colonización endomicorrízica de árboles de Swietenia humilis.
La respuesta de una plántula a una práctica cultural determinada es muy compleja y para el caso de los tratamientos evaluados, la sola adición de los dos sustratos pudo dar lugar a múltiples condiciones. A partir de las variables evaluadas, se observó cómo la especie caoba antillana mostró una tendencia, la cual indica que hay una respuesta diferenciada hacia las cepas de HMA y el tipo de sustrato aplicado.
Tanto los resultados del presente trabajo como los reportados en la bibliografía permiten afirmar que los biofertilizantes de tipo HMA representan un potencial para disminuir las limitantes en la producción de especies forestales a nivel de vivero. Que se refleja en un mayor desarrollo radical, mayor tasa de crecimiento, mejor adaptación a condiciones de estrés hídrico y nutricional en campo (Ramírez et al., 2018). Por otra parte, con base en HMA, el uso de biofertilizantes podría reducir los tiempos de vivero y para el productor forestal se convierten en mayor competitividad y sostenibilidad, con reducción de costos de producción y mejora en los ingresos.
La interacción del sustrato S2 conformado por 60 % de fibra de coco + 20 % de cascarilla de cacao + 20 % de aserrín de pino y las cepas micorrízicas Glomus cubense, Rhizoglomus intraradices y Funneliformis mosseae, son las más beneficiosas para la estimulación del crecimiento de la planta S. mahagoni cultivada vivero. Las cepas micorrízicas G. cubense y R. intraradices, ambas inoculadas en el sustrato S2, favorecieron la calidad de la planta S. mahagoni. La inoculación de sustratos orgánicos con Hongos Micorrízicos Arbusculares como biofertilizantes, demuestran ser alternativas viables para utilizar en la producción de plantas forestales de S. mahagoni.
6. Ética y conflicto de intereses
Las personas autoras declaran que han cumplido totalmente con todos los requisitos éticos y legales pertinentes, tanto durante el estudio como en la producción del manuscrito; que no hay conflictos de intereses de ningún tipo; que la entidad participante se menciona completa y claramente en la sección de agradecimientos; y que están totalmente de acuerdo con la versión final editada del artículo.
Los autores expresan su agradecimiento al personal del Centro de Estudios de Tecnología Agroforestal de la UG por su apoyo en las diversas etapas de esta investigación. Además, a las personas revisoras anónimas y la Revista por sus valiosos aportes para mejorar el presente artículo.
Abad, M., Fornes, F., Garrión, C., & Noguera, V. (2005). Physical properties of various coconut coir dusts compared to peat. HortScience, 40(7), 38-44.
https://doi.org/10.21273/HORTSCI.40.7.2138
Acosta, D. (2019). Aplicación de hongos micorrízicos arbusculares en la producción de plantas de selva baja caducifolia con fines de reforestación. [Tesis de maestría]. Universidad Autónoma del Estado de Morales, México. http://riaa.uaem.mx/xmlui/bitstream/handle/20.500.12055/713/AOPDXN05T.pdf?sequence=1&isAllowed=y
Arévalo, M., Oberpaur, C., & Méndez, C. (2016). Inclusión de musgo (Sphagnum magellanicum Brid.) y fibra de coco como componentes orgánicos del sustrato para almácigos de kiwi (Actinidia deliciosa). Idesia (Arica), 34(2), 47-55. http://doi.org/10.4067/S0718-34292016005000007
Bango, J. C., Pérez, L., & Torres, L. M. (2013). Alternativas biológicas para la obtención de posturas de caoba antillana en la etapa de vivero. DELOS: Revista Desarrollo Local Sostenible, 6(16), 1-10. https://www.eumed.net/rev/delos/16/posturas-caoba-antillana.pdf
Barbón, R., Borroto, I., Quiala, E., & Pérez, M. (2013). Efecto de sorbitol y 6-BAP en la maduración y germinación de embriones somáticos Swietenia mahagoni (L.) Jacq. Biotecnología Vegetal, 13(1), 51-55. https://revista.ibp.co.cu/index.php/BV/article/view/94
Betancourt, A. (1999). Silvicultura especial de árboles maderables tropicales. Editorial Científico-Técnica.
Bustamante, C. A., & Rojas. M. (2017). Efecto de las cepas de micorrizas y la riqueza del sustrato en el crecimiento de posturas de Theobroma cacao L. y los índices de utilización de nutrientes. Café Cacao, 16 (1), 22-34. http://www.inaf.co.cu/revistas/revista-cafe-cacao
Dickson, A., Leaf, A., Hosner. I. (1960). Quality appraisal of White Spruce and White Pine seedlings stock in nurseries. Forestry Chronicle, 36(1), 10-13. http://doi.org/10.5558/tfc36010-1
Falcón, E., Cobas, M., Bonilla, M., Rodríguez, O., Castillo, C. V., Rodríguez, E. (2019). Influencia del sustrato en la calidad de la planta Swietenia mahagoni (L.) Jacq. cultivada en tubetes. Revista Cubana de Ciencias Forestales, 7(3), 283-96. http://cfores.upr.edu.cu/index.php/cfores/article/view/422
Falcón, E., Cobas, M., Bonilla, M., Romero, C. V. (2018). Aplicación combinada de EcoMic® y Fitomas-E® en la calidad de la planta Swietenia mahagoni L. Jacq. Revista Forestal Baracoa, 37 (Número especial), 1-10. http://www.inaf.co.cu/revistas/revista-forestal-baracoa
Falcón, E., Rodríguez, O., Riera, M. C. (2013). Efecto de la inoculación de hongos micorrizógenos sobre la producción de posturas forestales en dos tipos de suelos. Revista Cultivos Tropicales, 34 (3), 32-39. http://doi.org/10.13140/RG.2.2.34452.30087
Feijen, F. A. A., Vos, R. A., Nuytinck, J., Merck. V. F. S. T. (2018). Evolutionary dynamics of mycorrhizal symbiosis in land plant diversification. Scientific Reports, 8(1), 1-7.
http://doi.org/10.1038/s41598-018-28920-x
Fernández, F., Gómez, R., Vanegas, L., Noval, B. M., Martinez, M. A. (2001). Producto inoculante micorrizógeno. Oficina Nacional de Propiedad Industrial. Cuba, Patente, 22641.
Gómez, M., De la Barrera, E., Villegas, J., Lindig, R. (2013). Fertilización y asociación con especies pioneras herbáceas en el crecimiento de Pinus pseudostrobus. Phyton, 82, 135-143. https://doi.org/10.32604/phyton.2013.82.135
Instituto de Meteorología de Cuba [INSMET] (2019). Centro Meteorológico Provincial de Guantánamo. http://www.guantanamo.gob.cu/es/centro-meteorologico-provincial-guantanamo
Jones, D. L., Hodge, A., Kuzyakov, Y. (2004). Plant and mycorrhizal regulation of rhizodeposition. New Phytologist, 163(3), 459-480. http://doi.org/10.1111/j.1469-8137.2004.01130.x
Klein, C. (2015). Substratos alternativos para produção de mudas. Revista Brasileira de Energias Renováveis, 4(3), 43-63. https://revistas.ufpr.br/rber/article/view/40742/pdf_64.
https://doi.org/10.5380/rber.v4i3.40742
Li, Z., Liu, L., Chen, J. y Teng, H. H. (2016). Cellular dissolution at hypha-and spore-mineral interfaces revealing unrecognized mechanisms and scales of fungal weathering. Geology, 44(4), 319-322. http://doi:10.1130/G37561.1
Oros, I., López, A. A., Moreno, J. P. Collado, J. C., Lara, L. A., Martínez, S. E., Solís, L. Y., Torres, A. A. (2015). Respuesta de plántulas de” Cedrela odorata” a la inoculación con Rhizophagus intraradices y diferentes niveles de defoliación. Revista Mexicana de Ciencias Agrícolas, 6(3), 627-635. https://doi.org/10.29312/remexca.v6i3.645
Panduro, M. E. (2017). Manejo de regeneración natural, en vivero, de Virola elongata (Benth) Warb. “Cumala blanca”, utilizando sustratos orgánicos. [Tesis de licenciatura]. UNAP.
https://repositorio.unapiquitos.edu.pe/bitstream/handle/20.500.12737/4890/Manuel_Tesis_Titulo_2017.pdf?sequence=1&isAllowed=y
Ramírez, M. M., Peñaranda, A. M., Pérez, U. A., Paola, D. (2018). Biofertilización con hongos formadores de micorrizas arbusculares (HFMA) en especies forestales en vivero. Biotecnología en el Sector Agropecuario y Agroindustrial, 16(2), 15-25.
https://revistas.unicauca.edu.co/index.php/biotecnologia/article/view/1162
Ricardo, N. E., Puentes, D. A., Torres, Y. A. (2016). Relaciones entre las características morfológico-funcionales y ecológicas de especies autóctonas de meliáceas cubanas: estrategia para su empleo forestal. Acta Botánica Cubana, 215(1), 2-23.
https://www.revista.geotech.cu/index.php.abc
Rodríguez, V. H. (2010). Diversidad de hongos micorrízico arbusculares y sus interacciones con factores ambientales y fisiológicos en la producción de plántulas de caoba. [Tesis de maestría]. Colegio Posgraduados de Veracruz. https://1library.co/document/wyeel81y-diversidad-micorrizicos-arbusculares-interaccion-ambientales-fisiologicos-produccion-macrophylla.html
Rodríguez, Y., Dalpé, Y., Séguin, S., Fernández, K., Fernández, F., Rivera, R. A. (2011). Glomus cubense sp. nov., an arbuscular mycorrhizal fungus from Cuba. Mycotaxon, 118(1), 337-347. http://doi.org/10.5248/118.337
Rueda, A., Orozco, G., Benavides, J. de D., Saenz, J., Muñoz, H., Prieto, J. Á. (2014). Calidad de planta producida en los viveros forestales de Nayaritt. Revista Mexicana de Ciencias Forestales, 5(22), 58-73. https://doi.org/10.29298/rmcf.v9i47.163
Santin, M., Maluche, C.R., Salengue, L., Kraft, E., Ogliari, A. J. (2018). Crescimento de mudas de canafístula com o uso de adubação biológica e bioestimulante em diferentes substratos. Enciclopedia Biosfera, 15(27), 95-106. https://doi.org/10.18677/EnciBio_2018A32
Schüßler, A., Walker, C. (2011). Evolution of the “Plant- Symbiotic” Fungal Phylum, Glomeromycota, [en línea]. En S.Pöggeler y J. Wöstemeyer (Eds.), Evolution of Fungi and Fungal-Like Organisms. Editorial Springer, Heidelberg, 163-185.
http://doi.org/10.1007/978-3-642-19974-5_7
Smith, S. E., Smith, F. A. (2011). Roles of Arbuscular Mycorrhizas in Plant Nutrition and Growth: New Paradigms from Cellular to Ecosystem Scales. Annual Review of Plant Biology, 62, 227-250. https://doi.org/10.1146/annurev-arplant-042110-103846
Souza, R. C. de, Pereira, M. G., Giácomo, R. G., Ribeiro da Silva, E.M., Tavares de Menezes, L. F. (2009). Produção de mudas micorrizadas de Schinus terebinthifolius Raddi. em diferentes substratos. Floresta, 39(1), 197-206. https://doi.org/10.5380/rf.v39i1.13739
1 Profesor en la Facultad Agroforestal, Universidad de Guantánamo (UG), Cuba; emir@cug.co.cu, https://orcid.org/0000-0001-8833-4942
2 Investigadora en el Centro de Estudios de Ciencias Forestales, Universidad de Pinar del Río (UPR) “Hermanos Saiz Montes de Oca”, Cuba; mcobas@upr.edu.cu; https://orcid.org/0000-0002-3785-5235
3 Profesora en la Facultad de Ciencias Forestales y Agropecuarias, Universidad de Pinar del Río (UPR) “Hermanos Saiz Montes de Oca”, Cuba; mbon@upr.edu.cu; https://orcid.org/0000-0002-6605-5296
4 Profesora en la Facultad Agroforestal, Universidad de Guantánamo (UG), Cuba; orfelina@cug.co.cu; https://orcid.org/0000-0002-1575-1515
5 Profesora en la Facultad de Educación, Universidad de Guantánamo (UG), Cuba; caridadrc@cug.co.cu;
https://orcid.org/0000-0002-8765-9777
6 Profesor adjunto en el Centro Universitario Municipal El Salvador, Universidad de Guantánamo (UG), Cuba; eliobinrodriguez@gmail.com;
https://orcid.org/0000-0002-5830-7289
Escuela de Ciencias Ambientales,
Universidad Nacional, Campus Omar Dengo
Apartado postal: 86-3000. Heredia, Costa Rica
Teléfono: +506 2277-3688
Correo electrónico revista.ambientales@una.ac.cr



