e-ISSN: 2215-3896.
(Julio-Diciembre, 2023). Vol 57(2)
DOI: https://doi.org/10.15359/rca.57-2.7
Open Acces: www.revistas.una.ac.cr/ambientales
e-Mail: revista.ambientales@una.cr
Licencia: CC BY NC SA 4.0
Evaluación del uso de la radiación UV y ozono en la degradación de metilparabeno
Evaluation of the use of UV radiation and ozone in the degradation of methylparaben
Yesmmy Karine Álvarez-Gómez1, Daniel Ricardo Delgado2
[Recibido: 11 de octubre 2022, Aceptado: 26 de enero 2023, Corregido: 18 de abril 2023, Publicado: 12 de mayo 2023]
Resumen
[Introducción]: Los contaminantes emergentes (CEs) son ahora tema de interés para diversas áreas de investigación científica. Se identifican en su mayoría estudios internacionales, sin embargo, aún se carece de información suficiente sobre los verdaderos efectos de estos compuestos en el ambiente y en la salud de las poblaciones en contacto con este tipo de contaminantes, a su vez se requiere la búsqueda y ejecución de tratamientos efectivos para minimizar su bioacumulación en el entorno, especialmente de aquellas sustancias de origen farmacéutico, las cuales ya están siendo reconocidas por su alto grado de toxicidad. [Objetivo]: En la presente investigación se estudió la degradación del contaminante emergente metilparabeno. [Metodología]: Para dicho estudio se contaminó el agua destilada, posteriormente se llevó a cabo el análisis de la efectividad del ozono, la radiación ultravioleta y el tratamiento combinado de radiación UV y ozonización en la degradación de la sustancia de origen farmacéutico. [Resultados]: En el estudio se encontró que el tratamiento combinado de radiación UV y ozonización fue más efectivo en la degradación del metilparabeno, en comparación con las técnicas de radiación UV y Ozono utilizadas por separado. [Conclusiones]: Los resultados obtenidos en la presente investigación generan información respecto a una nueva alternativa que permite la degradación de contaminantes farmacéuticos, como el metilparabeno, con el fin de minimizar el impacto ambiental de este tipo de sustancias.
Palabras claves: Contaminantes emergentes; fármacos; tratamiento de aguas; ozonización; radiación UV.
Abstract
[Introduction]: Contaminants of emerging concern (CECs) are now a subject of interest for various areas of scientific research, mostly international studies are identified, however, there is still insufficient information on the true effects of these compounds on the environment and on the health of populations that they are in contact with this type of contaminants, requiring in turn the search and execution of effective treatments to minimize their bioaccumulation in the environment, especially those substances of pharmaceutical origin, which are already being recognized for their high degree of toxicity. [Objective]: In the present investigation the degradation of the emerging contaminant methylparaben was studied. [Methodology]: For this study, the distilled water was contaminated, after which the analysis of the effectiveness of ozone, ultraviolet radiation, and the combined treatment of UV radiation and ozonation in the degradation of the substance of pharmaceutical origin was carried out. [Results]: In the study it was found that the combined treatment of UV radiation and ozonation was more effective in the degradation of methylparaben, compared to the techniques of UV and Ozone radiation used separately. [Conclusions]: The results obtained in this research generate information regarding a new alternative that allows the degradation of pharmaceutical contaminants, such as methylparaben, to minimize the environmental impact of this type of substance.
Keywords: Emerging contaminants; drugs; water treatment; ozonation; UV radiation.
Los parabenos son ésteres del ácido parahidroxibenzoico (p-HBA). Actualmente estos compuestos son ampliamente utilizados como conservantes en cosméticos, artículos de tocador, productos farmacéuticos y productos alimenticios, donde el metilparabeno (MeP) y propilparabeno son frecuentemente más utilizados (Haman et al., 2015; . Aunque los parabenos se consideran, en general, seguros, varios estudios sugirieron que podrían actuar como disruptores endocrinos, al producir actividad estrogénica , y podrían ser carcinógenos potenciales .
Los parabenos son moderadamente solubles en agua (con un rango de 160 µg/ml para bencilparabeno a 2 500 mg/ml para MeP, a 25 °C), aunque su solubilidad disminuye a medida que aumenta la cadena alquílica del parabeno (Cardenas et al., 2017; . La permeabilidad de los parabenos a través de la piel de los organismos y su asimilación en el tejido depende de la longitud de la cadena y de la formulación del producto, disminuye a medida que aumenta la longitud de la cadena del éster . Por el contrario, su toxicidad aumenta al aumentar la longitud de la cadena .
Debido a su uso generalizado, la aparición de parabenos en ambientes acuáticos, incluidos los ambientes marinos es frecuente. En el caso de MeP (Figura 1), se han encontrado promedios de 8.8 y 26 ng/L (Jonkers et al., 2010), y se han informado concentraciones que oscilan entre 3.02 y 31.7 ng/L en el agua costera de Florida USA. (Xue et al., 2017). Además, MeP es el parabeno principal detectado en organismos acuáticos. Los estudios de peces silvestres en todo el mundo revelan altas concentraciones de parabenos, especialmente MeP (hasta 80 %) en sus tejidos (Ramaswamy et al., 2011), que muestran la presencia ubicua de estos compuestos en el medio ambiente acuático. Además, los niveles detectados son más altos en adultos que en peces jóvenes (más del doble), lo que indica una bioacumulación de estos compuestos. Xue et al. (2015), Xue y Kannan (2016) encontraron grandes acumulaciones de parabenos, incluidos MeP y sus metabolitos en mamíferos marinos, peces y aves; así como el potencial de biomagnificación de MeP en una red alimentaria marina. Además, varios estudios muestran que los parabenos causan toxicidad aguda (Kamaya et al., 2015) y crónica en invertebrados acuáticos, incluidos los crustáceos (Terasaki et al., 2013).
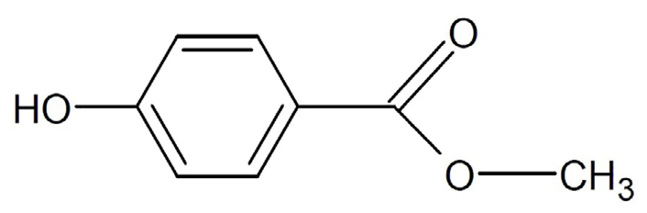
Figura 1. Estructura molecular del metilparabeno (Nombre IUPAC: Metil 4 – hidroxibenzoato, formula química: C8H8O3, Número CAS: 99-76-3).
Figure 1. Molecular structure of methylparaben (IUPAC name: Methyl 4 – hydroxybenzoate, chemical formula: C8H8O3, CAS number: 99-76-3).
Se agudiza la problemática anteriormente descrita porque los contaminantes emergentes no cuentan con un control legal sobre su vertimiento o el uso moderado de estas mismas, por lo cual se precisa una atención especial por parte de la comunidad científica para conocer sus verdaderos efectos sobre la biota y, así, poner en marcha tratamientos que permitan su adecuada depuración en los ecosistemas (Caviedes et al., 2017). Jiménez (2011) argumenta que los fármacos se diferencian de otras sustancias en el agua, ya que presentan una actividad biológica sobre diferentes organismos, debido a que sus propiedades fisicoquímicas facilitan su persistencia y bioacumulación.
Los fármacos son producidos para causar efectos farmacológicos en los seres vivos, por lo tanto, no es de extrañar que diversas investigaciones estén demostrando su nocividad en la biota y sus consecuencias adversas en los ecosistemas (Barceló et al., 2016; ; .
Aunque los parabenos son contaminantes relativamente nuevos, algunas investigaciones ya han demostrado su toxicidad y, por ende, la necesidad de regular sus usos en la industria, puesto que por sus propiedades antibacterianas y anti fungicidas, además de su bajo costo y fácil producción son unos de los fármacos más utilizados como conservantes (Caviedes et al., 2017c). En estudios realizados en Estados Unidos de América (EE. UU.) se pudo constatar que, de un total de 22 228 productos, el metilparabeno estaba presente en 7 866, el etilparabeno en 2 310, el propilparabeno en 6 260 y el butilparabeno en 2 784. (Lundov et al., 2009).
La problemática ambiental de fármacos en los ecosistemas colombianos evidentemente presenta grandes vacíos, tanto en sus potenciales efectos, como en los tratamientos necesarios para su degradación. Al no existir ninguna regulación específica sobre productos farmacéuticos en el ambiente acuático, teniendo en cuenta únicamente la prevención y gestión empresarial o institucional, se resta importancia al control de dichos residuos peligrosos (Caviedes et al., 2017; Caviedes & Delgado, 2015).
Conviene subrayar la necesidad apremiante de propiciar más investigaciones científicas, que den paso a la implementación de métodos eficientes con el entorno para el uso adecuado de las sustancias de origen farmacéutico y su oportuno tratamiento en el recurso hídrico, así mismo, sería oportuno que la comunidad científica proyecte a futuro el dar trascendencia a los resultados obtenidos referente a las técnicas propuestas, entre otras, para la depuración de estos contaminantes en ambientes edáficos en contacto con aguas contaminadas, teniendo en cuenta que el suelo es otro recurso vital para la sostenibilidad de la biota.
Para este estudio fueron evaluadas tres técnicas, radiación UV, ozonización y radiación UV y Ozono, para la degradación del metilparabeno presente en agua destilada, previamente contaminada. Los estudios de degradación iniciaron con ensayos preliminares a partir de cromatografía líquida de alta eficiencia y posteriormente por espectrofotometría UV-vis, a la espera de encontrar cuál de las tres técnicas propuestas presenta mayor efectividad en la degradación del fármaco estudiado.
Los reactivos utilizados para la preparación de soluciones y evaluación de las técnicas fueron de calidad HPLC: metilparabeno (Sigma-Aldrich), metanol, etanol (Merck), acetonitrilo (Merck). Agua destilada (Laboratorio de Química UCC). Material de laboratorio de vidrio (vasos de precipitado, agitadores, placas de Petri, pipetas, balones aforados).
Los equipos utilizados para los procedimientos analíticos en la evaluación de cada una de las técnicas y sustancias de interés fueron: espectrofotómetro UV-Vis, equipo HPLC cromatógrafo líquido modular Agilent 1200 Series, con automuestrador Agilent 1260 Infinity, desgasificador Agilent 1200 Series, bomba cuaternaria Agilent 1200 Series, Detector UV – vis con arreglo de diodos e integrados Agilent 1200 Series, Columna Eclipse XDB-C18 (150 mm x 4.6 mm, 3.5-5 µm). Reactor ozono y UV, baño de recirculación termostático, balanza analítica con precisión (0.1 mg).
El método de análisis de la concentración de cada una de las muestras se realizó mediante espectrofotometría UV, de manera similar a la empleada en múltiples trabajos desarrollados en el grupo de investigación (Ruidiaz et al., 2010).
2.3.1Preparación de soluciones
Preparación de 500 mL de solución con una concentración de 25 µg/mL de metilparabeno. Se toma muestra de 0.0125 g del metilparabeno y se afora a 500 mL con agua destilada.
2.3.2Evaluación de técnicas en la degradación de fármacos
Degradación del fármaco con UV: en un reactor aislado a la luz y termostatizado a 25 ºC fue irradiada la solución del fármaco por una lámpara de mercurio de 120 watts (rango de longitud de onda aproximada 350 nm -750 nm), se irradia luz en el espectro UV durante 90 minutos. Se tomaron muestras cada 5 minutos durante los primeros 30 minutos, luego cada 10 minutos durante los 60 minutos restantes.
Degradación del fármaco con ozono: en un reactor aislado a la luz y termostatizado a 25 ºC, se burbujeó ozono a la solución de estudio (ozono 80 mg/L), tomando las muestras en los mismos tiempos trabajados durante la técnica con UV.
Degradación del fármaco con UV y ozono: se repitió el procedimiento descrito en la técnica de ozono (ozono 80 mg/L), adicionando al reactor la lámpara UV (rango de longitud de onda aproximada 350 nm -750 nm).
2.3.3Análisis de muestras por cromatografía líquida de alta eficiencia (CLAE)
Con el ánimo de verificar si los productos de degradación absorbían a la longitud de onda de máxima absorbancia del fármaco en estudio, mediante cromatografía líquida de alta eficiencia se determinó, inicialmente, el tiempo de retención y pureza pico de un patrón. Posteriormente se realizaron corridas del fármaco expuesto a radiación ultravioleta y ozono, durante diferentes tiempos para identificar el comportamiento cromatográfico de las muestras.
Condiciones CLAE-DAD (cromatografía líquida de alta eficiencia con dispositivo de arreglo de diodos) (Delgado et al., 2014): se empleó un cromatógrafo líquido modular Agilent 1200 Series, con automuestreador Agilent 1260 Infinity, desgasificador Agilent 1200 Series, bomba cuaternaria Agilent 1200 Series, detector UV/VIS con arreglo de diodos e integrador Agilent 1200 Series, así como una columna eclipse XDB-C18 (150 mm x 4.6 mm, 3.5-5 µm) cuya temperatura de operación fue de 25 °C. El volumen de inyección fue de 10 µl (solución de 25 μg /mL); la fase móvil utilizada fue sistema de gradiente lineal de dos solventes agua/acetonitrilo, ambos con ácido trifluoroacético (TFA) al 0.05 % cuya composición de partida fue 90/10 a cero minutos, luego se cambió a 85/15 a los diez minutos. La velocidad de flujo fue de 2.5 ml/min, y la longitud de onda empleada para la cuantificación fue de 256 nm para el metilparabeno; con un ancho de pico de 0.1 minutos, en un rango de escaneo de 190 a 400 nm y un ancho de banda de 1.0 nm con una apertura (slit) de 2 nm. Una vez realizados los diferentes ensayos experimentales, se concluye que los productos de degradación generados por la exposición del fármaco a radiación ultravioleta y ozono no absorben a la longitud de máxima absorbancia del analito. Conforme a lo anterior, la metodología analítica UV/Vis puede ser empleada para el análisis de gradación de la sustancia en estudio. De otro lado esta metodología tiene ventajas en cuanto a la reducción de residuos contaminantes y tiempo de análisis.
2.3.4Análisis de muestras por espectrofotometría UV-vis
Para la obtención de los espectros, antes de iniciar con los análisis del fármaco en estudio, se utilizó como blanco agua destilada, posteriormente se analizaron las 12 alícuotas de metilparabeno tomadas durante los 90 minutos de exposición a la técnica de radiación ultravioleta. Las primeras 6 muestras se tomaron cada 5 minutos durante los primeros 30 minutos, las otras alícuotas cada 10 minutos durante los 60 minutos restantes. Cada una de las muestras fue introducida a la celda de cuarzo de 10 mm y de manera inmediata puesta dentro del espectrofotómetro para su respectivo análisis. Se repitió el procedimiento descrito con cada una de las técnicas evaluadas.
3.1Degradación mediante UV y Ozono
3.1.1Análisis de productos de degradación por radiación UV y ozono del metilparabeno mediante cromatografía líquida de alta eficiencia (CLAE)
En relación con la cromatografía líquida de alta eficiencia se llevaron a cabo los análisis de las soluciones sometidas a degradación UV y Ozono, con el ánimo de verificar si los productos de degradación absorbían a la longitud de onda de máxima absorción, se tuvieron presente los espectros del fármaco correspondientes a 256 nm (Figura 2). Se realizaron ensayos tomando la sustancia expuesta a la técnica combinada, para generar productos de degradación.
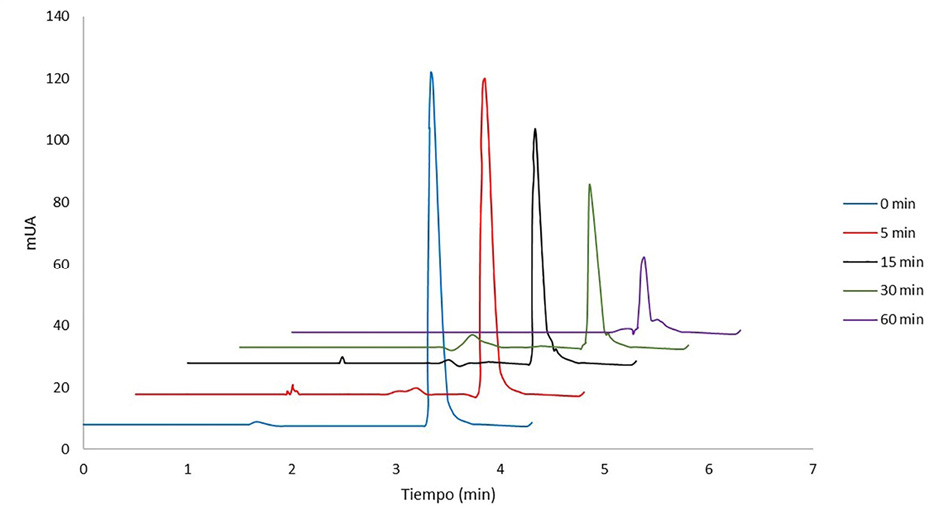
Figura 2. Cromatograma de metilparabeno sometido a degradación combinada UV y ozono a diferentes tiempos (0, 5, 15, 30 y 60 min) a temperatura ambiente con lambda máxima de 256 nm.
Figure 2. Chromatogram of Methylparaben subjected to combined UV and Ozone degradation at different times (0, 5, 15, 30 and 60 min) at room temperature with maximum lambda of 256 nm.
Cuadro 1. Áreas, tiempo de retención (TR) y factor de similitud o de pureza de pico del estándar de metilparabeno y de las muestras expuestas a condiciones de estrés (solución 25 μg/mL)
Table 1. Areas, retention time (RT) and peak similarity or purity factor of the methylparaben standard and of the samples exposed to stress conditions (25 μg/mL solution).
|
Fármaco |
Tiempo de exposición / minutos |
Absorbancia / mAU |
Tiempo de retención / minutos |
Pureza de pico / ‰ |
|
Metilparabeno |
0 |
854 |
3.45 |
999.95±0.01 |
|
5 |
745 |
3.57 |
995.83±0.01 |
|
|
15 |
523 |
3.42 |
990.42±0.01 |
|
|
30 |
201 |
3.33 |
984.25±0.01 |
|
|
60 |
78 |
3.54 |
975.25±0.01 |
En los cromatogramas correspondientes a una solución de metilparabeno de 25µg/mL, es evidente un solo pico donde los tiempos de retención estuvieron entre 3.33 y 3.57 minutos y la pureza de pico de 999.95 % equivalente a 99.995 % para tiempo cero, disminuye hasta 975.25 % equivalente a 97.525 % (Cuadro 1). El único pico de retención está indicando, posiblemente, la presencia de una sola sustancia mientras transcurre el tiempo de exposición del analito al tratamiento de luz UV y ozono, lo que permite interpretar que la lectura (λmax =256 nm) indica que los productos de degradación generados en la aplicación de la técnica no absorben o absorben a longitudes de onda diferentes a la de máxima absorbancia del fármaco. De otro lado, a medida que aumenta el tiempo de exposición del fármaco a la radiación ultravioleta y el ozono, la concentración de la sustancia se reduce. Esto se refleja en la disminución de la altura del pico o el área de este. Se observa, además, que, el metilparabeno presenta una degradación aproximada del 91 % durante los 60 minutos de exposición al tratamiento, calculados según la Ecuación 1:
Cálculo del porcentaje de degradación
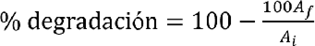 (E. 1)
(E. 1)
Donde:
Af: medida de la absorbancia de la muestra expuesta al tratamiento combinado de radiación UV y ozono a un tiempo t diferentes de cero.
Ai: medida de absorbancia de la muestra en el tiempo cero, es decir, a la muestra no expuesta al tratamiento, la cual para el presente caso corresponde a una muestra de concentración de 25 µg/mL.
3.1.2Análisis de la degradación por radiación UV del metilparabeno, mediante espectrofotometría UV
En la Figura 3, se presenta los espectros UV del proceso de degradación del metilparabeno expuesto a radiación ultravioleta.
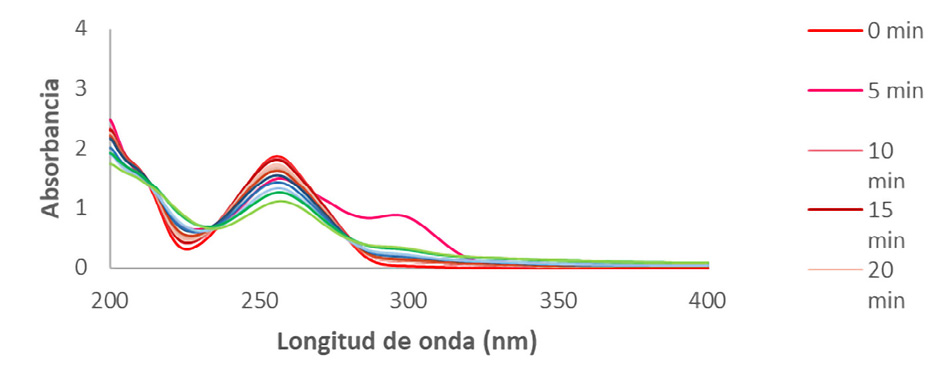
Figura 3. Espectros UV de metilparabeno sometido a degradación UV a diferentes tiempos (0, 5, 10, 15, 20, 25, 30, 40, 50, 60, 80 y 100 min) a temperatura ambiente.
Figure 3. UV spectra of Methylparaben subjected to UV degradation at different times (0, 5, 10, 15, 20, 25, 30, 40, 50, 60, 80 and 100 min) at room temperature.
Se observa que la absorbancia a la longitud de onda máxima (λmax =256 nm) disminuye respecto al tiempo de exposición, confirmándose así una degradación en esta sustancia. Los porcentajes de degradación fueron calculados (Ecuación 1) encontrándose un porcentaje del 47.31 % para el fármaco estudiado, al minuto 90 de exposición a la técnica UV.
3.1.3Análisis de la degradación por ozonización del metilparabeno mediante espectrofotometría UV
La Figura 4 representa los espectros ultravioletas del proceso de degradación del metilparabeno expuesto a ozonización.
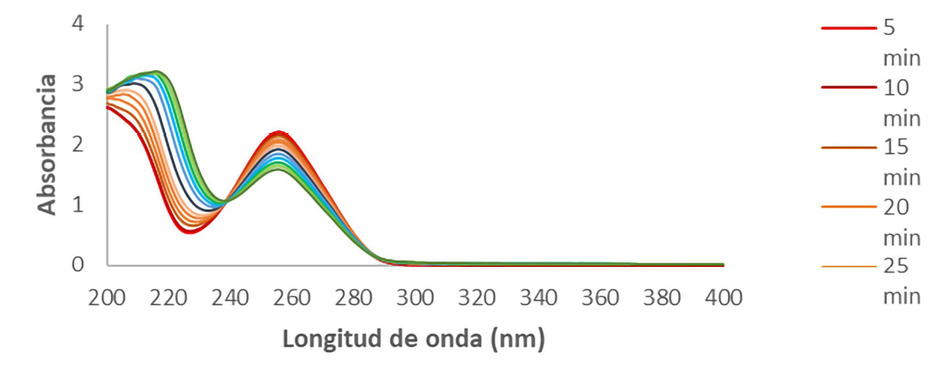
Figura 4. Espectros Uv de metilparabeno sometido a degradación ozono a diferentes tiempos (5, 10, 15, 20, 25, 30, 40, 50, 60, 70, 80 y 90 min) a temperatura ambiente.
Figure 4. Uv spectra of Methylparaben subjected to Ozone degradation at different times (5, 10, 15, 20, 25, 30, 40, 50, 60, 70, 80 and 90 min) at room temperature.
Se puede observar que, la diferencia respecto a la absorbancia de la banda principal (λmax =256 nm) con el espectro final es poco representativa. Esta información puede corroborarse teniendo en cuenta los porcentajes de degradación calculados (Ecuación 1), resulta importante resaltar que la técnica ozono presentó menor degradación, en comparación con la técnica UV. Por consiguiente, el porcentaje de degradación obtenido al minuto 90 de exposición al tratamiento con ozono fue de 28.12 %.
3.1.4Análisis de degradación por técnica combinada de radiación UV y ozonización, del metilparabeno mediante espectrofotometría UV
Se presentan los espectros ultravioleta del proceso de degradación del metilparabeno, expuesto a la técnica combinada (Figura 5).
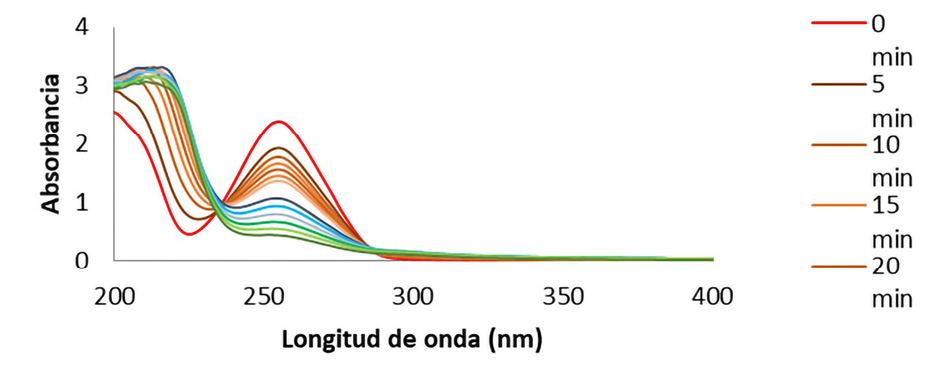
Figura 5. Espectros Uv de metilparabeno sometido a degradación mixta UV y ozono a diferentes tiempos (0, 5, 10, 15, 20, 25, 30, 40, 50, 60, 70, 80 y 90 min) a temperatura ambiente.
Figure 5. Uv spectra of Methylparaben subjected to mixed UV and ozone degradation at different times (0, 5, 10, 15, 20, 25, 30, 40, 50, 60, 70, 80 and 90 min) at room temperature.
Logra observarse mayor degradación del fármaco en comparación con las técnicas utilizadas por separado. En efecto, el metilparabeno alcanzó un porcentaje de degradación de 81.07 % a los 90 minutos de exposición con el tratamiento mixto. Esta técnica alcanzó a disminuir en grandes proporciones la concentración del fármaco, evidenciándose así, que la absorbancia de la banda principal (λmax = 256 nm) disminuye respecto al tiempo.
Referente al estudio de la cinética química, fueron evaluadas las técnicas de UV y ozono a diferentes temperaturas de 5 °C, 25 °C y 40 °C, para analizar, en función de esta variable, cuál podría presentar mayor degradación, teniendo en cuenta que la temperatura podría afectar la velocidad de las reacciones al aumentar la energía cinética de las moléculas que interfieren en el proceso de degradación de un fármaco. Conforme con los resultados obtenidos, donde a 25 °C se encontraron los mejores porcentajes de degradación para la sustancia en estudio, respecto a las tres técnicas evaluadas; la técnica combinada se llevó a cabo únicamente a temperatura de 25 °C. Para identificar el orden de la cinética de degradación del metilparabeno se utilizó el método gráfico, y se obtuvieron los coeficientes de correlación (Cuadros 2, 3 y 4).
Para la cinética de degradación del fármaco expuesto a la técnica de radiación UV, de acuerdo con el coeficiente de correlación de la ecuación, se presenta una cinética de degradación de segundo orden, lo que indica que la velocidad de reacción depende de la concentración del fármaco y es proporcional al cuadrado de la concentración del reactivo.
Cuadro 2. Coeficientes de las ecuaciones de orden 0, orden 1 y orden 2 para la cinética de degradación del metilparabeno por técnica UV, a 5, 25 y 40 °C (a = intercepto; b = constante; r2 = coeficiente de correlación)
Table 2. Coefficients of the equations of order 0, order 1 and order 2 for the degradation kinetics of methylparaben by UV technique, at 5, 25 and 40 °C (a = intercept; b = constant; r2 = correlation coefficient).
|
Orden de reacción |
T °C |
Coeficientes de la ecuación de la cinética de degradación |
||
|
Orden 0 |
|
a |
b |
r2 |
|
5 |
1.7016±0.0457 |
-0.0041±0.0004 |
0.8615 |
|
|
25 |
1.7626±0.0470 |
-0.0054±0.0005 |
0.8918 |
|
|
40 |
1.7626±0.0470 |
-0.0054±0.0005 |
0.8918 |
|
|
Orden 1 |
5 |
0.5411±0.026 |
-0.0031±0.0002 |
0.9013 |
|
25 |
0.6233±0.0201 |
-0.0047±0.0002 |
0.9737 |
|
|
40 |
0.6233±0.0201 |
-0.0047±0.0002 |
0.9737 |
|
|
Orden 2 |
5 |
0.5719±0.0131 |
0.0024±0.0001 |
0.9567 |
|
25 |
0.4902±0.0106 |
0.0042±0.0001 |
0.9908 |
|
|
40 |
0.4902±0.0106 |
0.0042±0.0001 |
0.9908 |
|
En cuanto al comportamiento cinético de la degradación por ozono, el metilparabeno presenta un orden definido para la reacción a 25 °C de orden 2; sin embargo, a 5 y 40 °C, se infiere que se presentan seudoórdenes dos y cero respectivamente, lo cual indica que a 40 °C la velocidad de reacción no depende de la concentración. Esto puede deberse a que la solubilidad del ozono, además de depender de la presión, la cual en este caso es contante (presión atmosférica), depende de la temperatura, lo que evidentemente afecta el orden de la reacción.
Cuadro 3. Coeficientes de las ecuaciones de orden 0, orden 1 y orden 2 para la cinética de degradación del metilparabeno por técnica ozono, a 5. 25 y 40°C (a = intercepto; b = constante; r2 = coeficiente de correlación)
Table 3. Coefficients of the equations of order 0, order 1 and order 2 for the degradation kinetics of methylparaben by Ozone technique, at 5, 25 and 40°C (a = intercept; b = constant; r2 = correlation coefficient).
|
Orden de reacción |
T °C |
Coeficientes de la ecuación de la cinética de degradación |
||
|
Orden 0 |
|
a |
b |
r2 |
|
5 |
2.0122±0.0690 |
-0.0193±0.0014 |
0.9415 |
|
|
25 |
2.2357±0.0078 |
-0.0074±0.0001 |
0.9954 |
|
|
40 |
2.2475±0.0154 |
-0.0023±0.0003 |
0.8290 |
|
|
Orden 1 |
5 |
0.7890±0.0044 |
-0.0013±0.00009 |
0.9469 |
|
25 |
2.2357±0.0078 |
-0.0074±0.0001 |
0.9954 |
|
|
40 |
0.8108±0.0074 |
-0.0011±0.0001 |
0.8234 |
|
|
Orden 2 |
5 |
0.4538±0.0020 |
0.0006±0.00004 |
0.9510 |
|
25 |
0.4378±0.0012 |
0.0020±0.00002 |
0.9985 |
|
|
40 |
0.4439±0.0035 |
0.0005±0.00007 |
0.8174 |
|
En cuanto al tratamiento combinado, la cinética de degradación del metilparabeno sigue un orden uno, por lo que la velocidad de degradación es proporcional a la concentración de fármaco.
Cuadro 4. Coeficientes de las ecuaciones de orden 0, orden 1 y orden 2 para la cinética de degradación del metilparabeno por técnica UV y Ozono, a 5. 25 y 40 °C (a = Intercepto; b = constante; r2 = coeficiente de correlación)
Table 4. Coefficients of the equations of order 0, order 1 and order 2 for the degradation kinetics of methylparaben by UV and Ozone techniques, at 5, 25 and 40 °C (a = intercept; b = constant; r2 = coefficient of correlation).
|
T °C |
Orden de reacción |
Coeficientes de la ecuación de la cinética de degradación |
||
|
25 |
|
a |
b |
r2 |
|
0 |
2.0122±0.0690 |
-0.0193±0.0014 |
0.9416 |
|
|
1 |
0.7963±0.0174 |
-0.0175±0.0003 |
0.9952 |
|
|
2 |
0.2993±0.0603 |
0.0184±0.0012 |
0.9504 |
|
3.3Degradación en función de la técnica
En la degradación del fármaco en estudio en función de la técnica, se realizó una gráfica con el fin de identificar y analizar los porcentajes de degradación calculados (Ecuación 1), respecto al tiempo de exposición del metilparabeno.
En la Cuadro 5 y la Figura 6, se observan los porcentajes de degradación del metilparabeno en estudio, respecto a las tres técnicas evaluadas a temperatura ambiente.
Cuadro 5. Porcentaje de degradación de metilparabeno en función del tiempo para las técnicas UV y ozono, a temperatura ambiente
Table 5. Percentage of methylparaben degradation as a function of time for the UV and Ozone techniques, at room temperature.
|
Tiempo (min) |
UV |
Ozono |
UV y ozono |
|
0 |
0.00 |
0.00 |
0.00 |
|
5 |
0.00 |
1.19 |
19.25 |
|
10 |
2.03 |
3.32 |
25.80 |
|
15 |
3.35 |
5.41 |
30.34 |
|
20 |
7.16 |
7.43 |
34.39 |
|
25 |
10.08 |
9.91 |
39.03 |
|
30 |
12.59 |
12.82 |
42.53 |
|
40 |
17.07 |
16.41 |
55.40 |
|
50 |
22.92 |
19.15 |
60.96 |
|
60 |
29.10 |
22.53 |
66.96 |
|
70 |
33.09 |
25.28 |
72.31 |
|
80 |
40.83 |
28.13 |
77.38 |
|
90 |
47.32 |
35.21 |
81.08 |
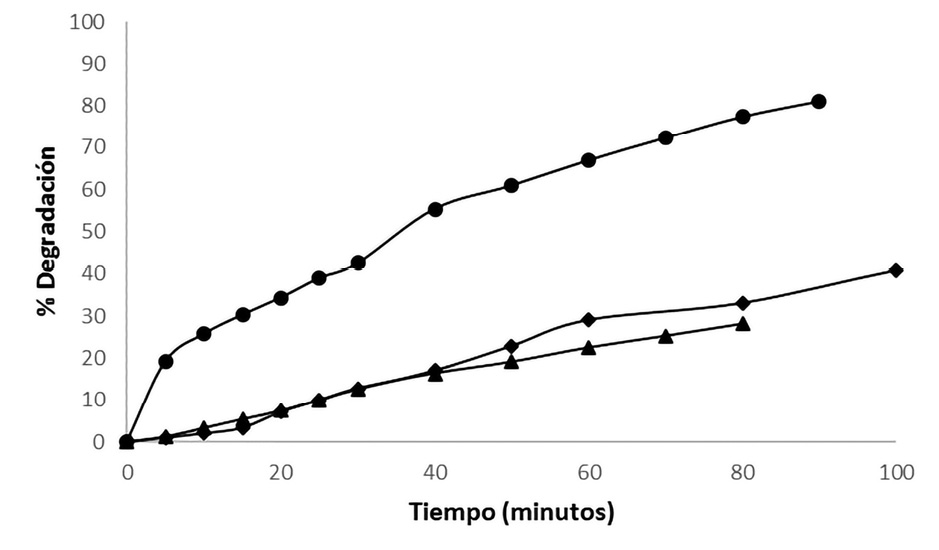
Figura 6. Porcentaje de degradación de metilparabeno, a temperatura ambiente (  = técnica UV;
= técnica UV;  = técnica ozono;
= técnica ozono;  = técnica combinada UV y ozono).
= técnica combinada UV y ozono).
Figure 6. Percentage of degradation of methylparaben, at room temperature ( = UV technique;
= UV technique;  = ozone technique;
= ozone technique;  = combined UV and ozone technique).
= combined UV and ozone technique).
Al graficar la degradación en función del tiempo para metilparabeno, de acuerdo con las técnicas empleadas, en la Figura 6 se visualiza claramente la eficiencia del tratamiento combinado sobre la técnica de radiación UV y el ozono utilizados por separado. El menor porcentaje de degradación resultó con la técnica ozono alcanzando un 28.13 %, a continuación, la técnica UV 47.32 % y con una gran diferencia el tratamiento combinado, degradó en un 81.08 % el fármaco en estudio, todos los porcentajes fueron tomados del minuto 90 de exposición para cada tratamiento.
Prosiguiendo el análisis de las tres técnicas evaluadas y con el fin de realizar la comprobación estadística de la hipótesis, en la cual se plantea que el tratamiento mixto UV y Ozono presenta mayor efectividad en la degradación del metilparabeno, en comparación con los tratamientos UV y ozonización utilizados por separado; se aplicó, entonces, la prueba Kruskal – Wallis. La prueba de Kruskal–Wallis constituye una alternativa no paramétrica al análisis de varianza usual y se considera como una extensión del procedimiento de suma de rangos de Wilcoxon. La hipótesis nula para la prueba de Kruskal-Wallis es que no existe diferencia entre los tratamientos (m1 = m2 = …. = ma), mientras que la hipótesis alternativa es que exista diferencia entre al menos un par de tratamientos (mi ¹ mj). (Miller & Freund, 1989).
Para la selección de la prueba estadística se tuvo en cuenta que se trabajaron datos no paramétricos, se manejaron variables cuantitativas y se compararon más de dos grupos (Wackerly et al., 2002), es decir, los tres tratamientos evaluados para degradar el fármaco. En el estudio estadístico se consideraron las siguientes hipótesis, la hipótesis nula (H0) e hipótesis alterna (H1):
H0: los resultados de las pruebas en las tres técnicas evaluadas son iguales.
H1: los resultados de las pruebas en las tres técnicas evaluadas no son iguales.
De acuerdo con la prueba Kruskal – Wallis, se observa que existen diferencias estadísticamente significativas para los resultados obtenidos en las tres técnicas evaluadas frente a la degradación del metilparabeno. Dicho lo anterior, se muestra que para metilparabeno p = 0.0001; el valor de p, es decir, la significancia estadística es menor a 0.05 para la sustancia estudiada, por ende, dado este resultado se rechaza la hipótesis nula. En consecuencia, se acepta la hipótesis alterna, así se confirma que los resultados de las pruebas no son iguales, por lo cual sí existe una diferencia estadística significativa entre los tratamientos aplicados. En definitiva, según lo expuesto anteriormente en la degradación en función de las técnicas, confirmando también lo observado en la Figura 6; el tratamiento combinado UV y ozono presentó mayor efectividad en la degradación del metilparabeno presente en agua destilada, previamente contaminada.
El tratamiento combinado UV y ozonización obtiene la mejor efectividad en la degradación del metilparabeno comparado con las técnicas UV y ozono aplicadas por separado. De esta manera, la sustancia estudiada presenta un porcentaje de degradación de 81.08 % con la técnica combinada al minuto 90 de exposición al tratamiento. En el caso de la técnica con ozono, esta presenta mínima efectividad en la degradación del metilparabeno en comparación con la técnica de radiación UV, el porcentaje de degradación es 28.13 % durante los 90 minutos de exposición al tratamiento de ozonización y de 47.32 % durante la exposición a radiación UV. Estadísticamente, existen diferencias significativas entre los resultados obtenidos para cada técnica evaluada. Según la prueba aplicada de Kruskal – Wallis, los resultados de degradación para los tres tratamientos difieren entre sí, teniendo en cuenta que la significancia estadística fue menor a 0.05. Finalmente, los resultados obtenidos en la presente investigación generan información respecto a una nueva alternativa que permita la degradación de contaminantes farmacéuticos, como el metilparabeno, con el fin de minimizar el impacto ambiental de este tipo de sustancias.
Los autores expresan su agradecimiento a la Universidad Surcolombiana y la Universidad Cooperativa de Colombia por su gran apoyo en la logística de la presente investigación. Además, a las personas revisoras anónimas de la revista por sus aportes, los cuales enriquecieron el presente documento.
6.Ética y conflicto de intereses
Las personas autoras declaran que han cumplido totalmente con todos los requisitos éticos y legales pertinentes, tanto durante el estudio como en la producción del manuscrito; que no hay conflictos de intereses de ningún tipo; que todas las fuentes financieras se mencionan completa y claramente en la sección de agradecimientos; y que están totalmente de acuerdo con la versión final editada del artículo.
Arvelo, F., Sojo, F. y Cotte, C. (2016). Contaminación, disruptores endocrinos y cáncer. Investigación Clínica, (1), 77-92.
Barceló, D., Lopez de Alda, J., Petrovic, M., Lacorte, S. y Piña, B. (2016). Los contaminantes emergentes en los sistemas de saneamiento y sus efectos ambientales. Consejo Superior de Investigaciones Científicas, Departamento de Química Ambiental, Barcelona.
Cardenas, Z., Jiménez, D.M., Delgado, D. R., Almanza, O., Jouyban, A., Martínez, F., & Acree Jr. W.E. (2017). Solubility and preferential solvation of some n-alkyl-parabens in methanol + water mixtures at 298.15 K, The Journal of Chemical Thermodynamics, (108), 26-37. https://doi.org/10.1016/j.jct.2017.01.005
Cardenas, Z., Jiménez, D.M., & Martínez, F. (2015). Thermodynamic study of the partitioning of methyl and propyl parabens in some organic solvent/buffer systems. The Journal of Chemical Thermodynamics, (88), 180-187. https://doi.org/10.1016/j.jct.2015.03.006
Caviedes, D., Camacho-Feria, D. M. y Delgado, D. (2017a). Tratamientos para la remoción de antibacteriales y agentes antimicrobiales presentes en aguas residuales. Revista Logos Ciencia & Tecnología, (9), 43-62. https://doi.org/10.22335/rlct.v9i1.370
Caviedes, D. I., Delgado, D. R. y Olaya, A. (2017b). Remoción de metales pesados comúnmente generados por la actividad industrial, empleando macrófitas neotropicales. Producción+ Limpia, (11) 126-148. https://doi.org/10.22507/pml.v11n2a11
Caviedes, D. I., Delgado, D. R. y Olaya, A. (2017c). Normatividad ambiental dirigida a regular la presencia de los productos farmacéuticos residuales en ambientes acuáticos. Revista Jurídica Piélagus, (16) 121-130. https://doi.org/10.25054/16576799.1445
Caviedes, D., y Delgado, D. (2015). Regulación ambiental sobre los productos farmacéuticos residuales en ambientes acuáticos. Entornos, (28), 76-80. https://doi.org/10.25054/01247905.1225
Darbre, P. D., Aljarrah, A., Miller, W. R., Coldham, N. G., Sauer, M. J., & Pope, G. S. (2004). Concentrations of parabens in human breast tumours. Journal of Applied Toxicology, (24) 5-13. https://doi.org/10.1002/jat.958
Delgado, D. R., Caviedes-Rubio, D. I., Ortiz, C. P., Parra-Pava, Y. L., Peña, M. A., Jouyban, A., Mirheydari, S., Martínez, M., & Acree Jr, W.E. (2019). Solubility of sulphadiazine in (acetonitrile+ water) mixtures: measurement, correlation, thermodynamics and preferential solvation. Physics and Chemistry of Liquids. https://doi.org/10.1080/00319104.2019.1594227
Delgado, D. R., Rodríguez, G., Martínez, J.A., Rojas, J. H., & Martínez, F. (2014). Validación de una metodología analítica empleando espectrofotometría ultravioleta para el estudio de la solubilidad de algunas sulfonamidas en mezclas cosolventes alcohol+ agua. Revista Colombiana de Química, (43) 31-40. https://revistas.unal.edu.co/index.php/rcolquim/article/view/53429/52920
Delgado, H. (2016). Análisis de la exposición de compuestos emergentes en varios escenarios de usos del agua [Tesis de maestría]. Universidad Politécnica de Cataluña, Barcelona, España.
Elorriaga, Y., Marino, D., Carriquiribordi, P., & Ronco, A. (2012). Contaminantes emergentes: Productos farmacéuticos en el medio ambiente. La Plata, Argentina.
Gaviria-Castillo, A.C., Artunduaga-Tole, J. D., Rodríguez-Rubiano, J. D., Zuñiga-Andrade, J. A., Delgado, D. R., Jouyban, A. & Martínez, F. (2019). Solution thermodynamics and preferential solvation of triclocarban in {1, 4-dioxane (1)+ water (2)} mixtures at 298.15 K. Physics and Chemistry of Liquids, (57) 55-66. https://doi.org/10.1080/00319104.2017.1416613
Haman, C., Dauchy, X., Rosin, C., & Munoz, J. F. (2015). Occurrence, fate and behaviour of parabens in aquatic environments: a review. Water Research (68) 1-11. https://doi.org/10.1016/j.watres.2014.09.030
Jiménez, C. (2011). Contaminantes orgánicos emergentes en el ambiente: Productos farmacéuticos. Revista Lasallista de Investigación, 143-153.
Jonkers, N., Sousa, A., Galante-Oliveira, S., Barroso, C.M., Kohler, H.-P. E. & Giger, W. (2010). Ocurrence and sources of selected phenolic endocrine disruptors in Ria de Aveiro, Portugal. Environmental Science and Pollution Research, (17) 834-843. https://doi.org/10.1007/s11356-009-0275-5
Kamaya, Y., Fukaya, Y. & Suzuki, K. (2015). Acute toxicity of benzoic acids to the crustacean Dapnia magna Chemosphere, (59) 255-261. https://doi.org/10.1016/j.chemosphere.2004.11.003
Kusk, K. O., Krüger, T., Long, M., Taxvig, C., Lykkesfeldt, A. E., Frederiksen, H., Andersson, A. M., Andersen, H. R., Hansen, K. M., Nellemann, C., & Bonefeld-Jørgensen, E. C. (2011). Endocrine potency of wastewater: contents of endocrine disrupting chemicals and effects measured by in vivo and in vitro assays. Environmental Toxicology and Chemistry, (30) 413-426. https://doi.org/10.1002/etc.385
Lundov, M., Moesby, L., Zachariae, C., & Johansen, J. (2009). Contamination versus preservation of cosmetics: a review on legislation, usage, infections, and contact allergy. Contac Dermatitis, (60), 70-78. https://doi.org/10.1111/j.1600-0536.2008.01501.x
Miller, I. & Freund, J. (1989). Probabilidad y estadística para ingenieros, Capitulo 10.
Muñoz, A. (2017). Antibióticos en el suelo [Tesis de pregrado]. Universidad Complutense, Facultad de Farmacia, Madrid, España.
Peña, M. A., Delgado, D. R., & Martinez, F. (2015). Preferential solvation of some n-alkyl p-substituted benzoates in propylene glycol + water cosolvent mixtures. Physics and Chemistry of Liquids, (53), 455-466. https://doi.org/10.1080/00319104.2015.1006221
Ramaswamy, B. R., Kim, J.-W., Isobe, T., Chang, K.-H., Amano, A., Miller, T. W., Siringan, F. P., & Tanabe, S. (2011). Determination of preservative and antimicrobial compounds in fish from Manila Bay, Phillippines using ultra high performance liquid chromatography tandem mass spectrometry, and assessment of human dietary exposure. Journal of Hazardous Materials, (192) 1739-1745. https://doi.org/10.1016/j.jhazmat.2011.07.006
Romero-Nieto, A. M., Cerquera, N. E., Martínez, F. & Delgado, D. R (2019). Thermodynamic study of the solubility of ethylparaben in acetonitrile + water cosolvent mixtures at different temperatures. Journal of Molecular Liquids, (287), 110894. https://doi.org/10.1016/j.molliq.2019.110894
Ruidiaz, M. A., Delgado, D. R., Mora, C. P., Yurquina, A., & Martínez, F. (2010). Estimation of the indomethacin solubility in ethanol+ water mixtures by the extended Hildebrand solubility approach. Revista Colombiana de Ciencias Químico-Farmacéuticas, (39) 79-95.
Soler, A. (2016). Determinación de la toxicidad aguda de ingredientes utilizados en los productos de cuidado personal [Tesis de maestría]. Universidad Politécnica de Cataluña, Barcelona, España.
Terasaki, M., Abe, R., Makino, M. & Tatarazako, N. (2013). Chronic toxicity of parabens and their chlorinated by-products in Ceriodaphnia dubia. Environmental Toxicology, (30) 664-673. https://doi.org/10.1002/tox.21944
Wackerly, D., Mendenhall, W., & Sheaffer, R. (2002). Estadística matemática con aplicaciones. Cengage Learning Editores.
Xue, X., Xue, J., Liu, W., Adams, D. H., & Kannan, K. (2017). Trophic magnification of parabens and their metabolites in a subtropical marine food web. Environmental Science & Technology, (51) 780-789. https://doi.org/10.1021/acs.est.6b05501
Xue, J. & Kannan, K. (2016). Accumulation profiles of parabens and their metabolites in fish, black bear, and birds, including bald eagles and albatrosses. Environment International, (94) 546-553. https://doi.org/10.1016/j.envint.2016.06.015
Xue, J., Sasaki, N., Elangovan, M., Diamond, G., & Kannan, K. (2015). Elevated accumulation of parabens and their metabolites in marine mammals from the United States coastal waters. Environmental Science & Technology, (49) 12071-12079. https://doi.org/10.1021/acs.est.5b03601
1 Especialista en Ingeniería y Gestión Ambiental, Universidad Surcolombiana, Colombia. yag0531@hotmail.com; https://orcid.org/0000-0002-3588-741X
2 Docente investigador de la Facultad de Ingeniería, Programa de Ingeniería Civil, Universidad Cooperativa de Colombia, Colombia. drdelgado@unal.edu.co; https://orcid.org/0000-0002-4835-9739
Escuela de Ciencias Ambientales,
Universidad Nacional, Campus Omar Dengo
Apartado postal: 86-3000. Heredia, Costa Rica
Teléfono: +506 2277-3688
Correo electrónico revista.ambientales@una.ac.cr



