e-ISSN: 2215-3896.
(Enero-Junio, 2025). Vol 59 (1)
DOI: https://doi.org/10.15359/rca.59-1.5
Open Acces: www.revistas.una.ac.cr/ambientales
e-Mail: revista.ambientales@una.cr
Licencia: CC BY NC SA 4.0
Tratamiento químico de vinaza de caña de azúcar con peróxido de hidrógeno
Chemical treatment of sugar cane vinasse with hydrogen peroxide
Adriana Patricia del M. Chaile,1 María Emilia Uboldi,2 Mercedes Marta Elsa Ferreyra3
[Recibido: 19 de enero del 2024, Aceptado: 17 de julio del 2024, Corregido: 30 de julio del 2024, Publicado: 25 de septiembre del 2024]
Resumen
[Introducción]: La vinaza se genera como residuo en la producción de etanol por fermentación-destilación de melazas/jugos de caña de azúcar, a razón de 13 L/L de etanol. Es un efluente líquido, ácido caracterizado por una elevada mineralización y valores de demanda química de oxígeno (DQO) de hasta 150 000 mg/L, siendo altamente contaminante. [Objetivo]: Ealuar un proceso de tratamiento de vinazas con peróxido de hidrógeno, como fuente de radicales hidroxilos, en escala laboratorio. [Metodología]: Las muestras de vinazas, de destilerías de la provincia de Tucumán, se caracterizaron según técnicas normalizadas de Standard Methods. Los ensayos de oxidación se realizaron con distintas relaciones de peróxido/vinaza, en un reactor semibatch, en condiciones ambientales, midiendo DQO como parámetro indicador del tratamiento. [Resultados]: Al cabo de cinco días se logró una disminución de DQO del 85 % y un aumento del Índice de Biodegradabilidad. La cinética de la reacción oxidativa fue de primer orden respecto de DQO, con una constante aparente de velocidad de 0.3694 1/día. [Conclusiones]: Si bien no se lograron los valores de DQO permitidos por la normativa local (250 mg/L), el tratamiento propuesto es alentador por su simpleza, representando una opción potencial al desafío ambiental que representan las vinazas en América Latina.
Palabras clave: vinaza; efluente destilería; tratamiento oxidativo.
Abstract
[Introduction]: Vinasse is generated as a residue in the production of ethanol by fermentation-distillation of molasses/sugar cane juice, at a rate of 13 L/L of ethanol. It is an acid liquid, brown in color, characterized by high mineralization and Chemical Oxygen Demand (COD) values of up to 150 000 mg/L, being highly polluting. [Objective]: The objective of this research was to evaluate a vinasse treatment process with hydrogen peroxide as a source of hydroxyl radicals at laboratory scale. [Methodology]: The vinasse samples, from different distilleries in the province of Tucumán, were characterized following standardized techniques of Standard Methods. The oxidation tests were carried out with different peroxide/vinasses ratios, in a semi-batch reactor, under ambient conditions, measuring COD as an indicator parameter of the treatment. [Results]: After 5 days, an 85 % decrease in COD and an increase in the Biodegradability Index were achieved. The kinetics of the oxidative reaction was first order with respect to COD, with an apparent rate constant of 0.3694 1/day. [Conclusions]: Although the COD values allowed by local regulations (250 mg/L) were not reached, the proposed treatment is encouraging due to its simplicity, representing a potential option to the environmental challenge represented by vinaze in Latin America.
Keywords: vinasse; distillery effluent; oxidative treatment.
En Argentina, mediante la Ley 26093 (2006), Régimen de Regulación y Promoción para la Producción y Uso Sustentables de Biocombustibles, se estableció que todo combustible líquido caracterizado como nafta, deberá ser mezclado con bioetanol, en un porcentaje del 5 %. A partir de abril del 2016, el porcentaje de bioetanol por litro de nafta en Argentina aumentó al 12 % (Ministerio de Energía y Minería, 2016) y el Gobierno Nacional estableció que este volumen extra de bioetanol debía provenir exclusivamente de la caña de azúcar. Esto llevó a un incremento sustancial en la producción de etanol a partir de la fermentación de melazas y jugo de caña de azúcar, siendo Tucumán, provincia del noroeste argentino, el polo industrial de la región, capaz de responder a la demanda. De acuerdo con Chanfón-Curbelo y Lorenzo-Acosta (2014), los residuos industriales más contaminantes por su carga orgánica provienen de la industria alcoholera.
La vinaza es el efluente efecto de la producción de alcohol a partir de la fermentación-destilación de melaza y jugo de caña de azúcar. Es un residuo líquido de color marrón, con un gran contenido de sólidos suspendidos, olor a miel final y sabor a malta, presenta pH ácido, elevados valores de demanda química de oxígeno (DQO), entre 70 000 y 150 000 mg/L, y de demanda bioquímica de oxígeno (DBO), entre 35 000 y 60 000 mg/L. Aproximadamente la mitad de los sólidos se deben a compuestos no volátiles provenientes del caldo de fermentación, orgánicos no fermentescibles, compuestos fenólicos, polifenólicos y azúcares residuales (Sangave et al., 2007; Robles-Gonzalez et al., 2012); posee materiales orgánicos y nutrientes minerales que son parte de vegetales, como aminoácidos, proteínas, lípidos, ácidos diversos, enzimas, bases, ácidos nucleicos, clorofila, lignina, quinonas y ceras (Valeiro y Portocarrero, 2017); los valores de conductividad eléctrica y de porcentaje de cenizas indican la presencia de un elevado contenido de sales minerales (Ahmed et al., 2013). Además, en las columnas de destilación se obtiene como residuo vinaza en una proporción de 12 a 18 litros por cada litro de alcohol destilado, 96° G. L. (de la Cruz, 2002).
En tal sentido, durante el 2021 se produjeron en Tucumán un total de 310 846 m3 de etanol (Centro Azucarero Argentino, 2021), lo cual generó un volumen de alrededor de 4 000 000 m3 de vinaza (considerando 13 L vinaza/L etanol, como relación regional). Por ello, se considera como un residuo líquido que impacta de forma negativa el ambiente, en especial a los recursos hídricos, pues disminuye la luminosidad de las aguas, la actividad fotosintética y el oxígeno disuelto; además producen eutrofización, contribuye al aumento de poblaciones de insectos y vectores, y al desarrollo de enfermedades (Bermúdez et al., 2000). La provincia de Santiago del Estero enfrentó graves daños ecológicos en el embalse de Termas de Río Hondo, como contaminación de las aguas y mortandad de peces de todos los tamaños y especies, lo cual permite afirmaron que fue consecuencia del vertido de vinaza por las destilerías tucumanas en la cuenca Salí-Dulce.
Por su parte, Brasil es el mayor productor mundial de bioetanol a partir de caña de azúcar (24 %), seguido por Colombia (0.4 %); por lo que se evidencia un gran interés en desarrollar alternativas que mitiguen la contaminación de este subproducto en los países latinoamericanos, constituyendo un desafío en términos ambientales (Ospina-León et al., 2023).
En los últimos años todos los estudios sobre vinazas se centraron en su carga orgánica y elevada concentración de sales para un determinado uso final. En términos generales, en la región se aplican tres procesos principales de tratamiento de las vinazas: la fabricación de compost, donde se utiliza vinaza previamente concentrada y mezclada con remanentes del cultivo y procesamiento de la caña de azúcar (hojas y cachaza) para producción de abono (Lim et al., 2016); el uso de vinaza para fertirrigación, que requiere concentrar vinaza hasta cerca de 60° Brix, por lo que es elevado el consumo de energía (Sim y Wu, 2010) y, además, la aplicación sin control se tornó contraproducente para algunos tipos de suelos (Ospina-León et al., 2023); y el uso de vinaza como fuente energética por la vía de incineración, lo cual tiene como limitación la necesidad de trabajar a temperaturas inferiores a 700 °C (las sales de potasio se funden a esta temperatura) y el requerimiento energético para concentrar la vinaza.
Se han propuesto otros usos y tratamiento para la vinaza generada, por ejemplo, la biodigestión anaeróbica para obtener biogás, la producción de proteína unicelular y alimento animal (Christofoletti et al., 2013; Jiang et al., 2012; Laime et al.., 2011). Los altos costos de producción, altos costos energéticos, largos períodos de producción o la imposibilidad del uso de toda la vinaza generada, son algunas de las desventajas que han conducido a que estas alternativas no sean las más generalizadas (Cabrera, 2013; España-Gamboa et al., 2011; Pérez-Bermúdez y Garrido-Carraler, 2006; Satyawali y Balakrishnan, 2008).
En la actualidad, numerosos grupos de investigación y técnicos del sector apuntan su experiencia en lograr una solución económica y factible para la disposición final de vinazas, pues el volumen de esta se incrementa con el aumento en la producción de alcohol y excede cualquier uso propuesto hasta ahora.
Los procesos de oxidación avanzada (POA) resultaron ser uno de los métodos más eficientes para la remoción de contaminantes contenidos en aguas superficiales y subterráneas, así como en residuos industriales líquidos (García-Gámez et al., 2011). En general, se utilizan cuando los efluentes poseen contaminantes con alta estabilidad química o una baja biodegradabilidad (Poyatos et al., 2010).
La oxidación avanzada se basa en la generación de radicales hidroxilos, los cuales tienen un alto potencial rédox (2.9 V) y son capaces de destruir e incluso de mineralizar cualquier contaminante orgánico. Las reacciones químicas producidas se caracterizan por su no-selectividad y por elevada velocidad de reacción (Sanz, Lombraña y de Luis, 2013). Incluso, los radicales OH• pueden modificar la estructura química de los compuestos orgánicos recalcitrantes, convirtiéndolos en compuestos más simples, de menor masa molecular, menos tóxicos a los microorganismos y, en consecuencia, más biodegradables (Collins y Bolton, 2016) y se generan in situ por la aplicación directa o la combinación de agentes oxidantes como el ozono, el peróxido de hidrógeno, la radiación ultravioleta, las sales férrico/ferrosas, entre otras.
Al respecto, Sanz et al. (2013) presentaron un resumen de trabajos realizados desde el 2004, con ejemplos de aplicación de oxidación avanzada en el tratamiento de efluentes industriales con elevada carga orgánica. El proceso con peróxido de hidrógeno adquiere singular importancia, pues se trata de un oxidante económico que no genera residuos y tiene la capacidad de producir radical hidroxilo vía catálisis, incluso puede oxidar compuestos orgánicos complejos en compuestos menores, menos tóxicos y más biodegradables ajustando factores como el pH, temperatura, dosis, tiempo de reacción y adición de catalizadores (Stefan, 2017). Fenton (1894) fue el primero en describir la oxidación del ácido tartárico en presencia de peróxido de hidrógeno con iones ferroso, por lo que la oxidación de sustratos orgánicos e inorgánicos por hierro (II) y H2O2 es conocida como reacción de Fenton.
Estas reacciones ocurren también con iones metálicos de transición como Fe (III), Mn (II) o Cu (I), se las conoce como reacciones tipo Fenton (Doménech et al., 2001; Litter y Slodowicz, 2017) y se pueden representar como:
Mnn+ + H2O2 ® Me(n+1)+ + HO· + HO-
Por lo expuesto, el objetivo del presente trabajo fue evaluar un proceso de tratamiento de vinazas con peróxido de hidrógeno, aprovechando el contenido de iones metálicos como componentes naturales del efluente para producir reacciones de oxidación.
2.1Muestras de vinaza y su caracterización
Se trabajó con muestras de vinazas extraidas de la primera columna de destilación de cuatro instalaciones de producción de etanol (destilerías), anexas a ingenios azucareros ubicados en la zona oeste de la provincia de Tucumán. Estas se identificaron con las letras L, F, C y S.
Se determinaron los siguientes parámetros fisicoquímicos que permitieron caracterizar la vinaza, antes del tratamiento oxidativo: pH, conductividad eléctrica, demanda química de oxígeno (DQO), demanda bioquímica de oxígeno a los cinco días (DBO5) sólidos totales, sólidos sedimentables a las 2 hs., potasio, cobre, zinc, hierro. El contenido de sólidos disueltos se midió mediante la determinación de Brix usando un refractómetro de Abbé. Las determinaciones de DBO y de metales se realizaron en los laboratorios de la Sección Química del Área Industrial de la Estación Experimental Agroindustrial Obispo Colombres (EEAOC); el resto de los parámetros en el Laboratorio de Química General del Departamento de Ingeniería de Procesos y Gestión Industrial (Universidad Nacional de Tucumán). Las técnicas empleadas responden a Standard Methods for the Examination of Water and Wastewaters (APHA, 2005).
Las determinaciones de DQO se llevaron a cabo por el método colorimétrico de reflujo cerrado SM 5220D, con lecturas de absorbancia a 420 nm para rangos bajos y 600 nm para rangos altos. Se usó Microdigital Termoreactor DQO Modelo TR-105 y Espectrofotómetro UV-VIS Biotraza, Modelo 752. El método fue validado, resultando el límite de detección en 5 mg/L; límite de cuantificación de 15 mg/L; en dos rangos lineales, 15-200 mg/L y 200-1400 mg/L, con exactitud de hasta 5 mg/L, con CV % de hasta 7.5 %, en el rango 1 y 10 mg/L, con CV % hasta 6.5 %, en el rango 2; demostrando precisión aceptable en ambos rangos de trabajo.
En vinazas crudas y tratadas, se calculó el Índice de Biodegradabilidad (IB) como la relación entre DBO5/DQO Ardila et al. (2012) indicaron que la relación DBO5/DQO permite determinar la cantidad de materia orgánica e inorgánica contenida en una muestra de un efluente, que es susceptible de ser depurada en cinco días por los microorganismos. Así, cuando la relación DBO5/DQO es menor a 0.30, el efluente es en su mayoría no biodegradable, mientras que valores superiores a 0.70 favorecen las condiciones de recuperación por métodos biológicos.
2.2Tratamiento de vinaza por oxidación
Se usó una solución de peróxido de hidrógeno al 30 % m/v, como reactivo de oxidación. Los ensayos se llevaron a cabo a escala laboratorio, a 30 ºC y en un reactor semi batch con baño termostatizado.
Se sabe que el pH es uno de los factores importantes que controlan la eficiencia de las técnicas de oxidación avanzada, tal es así que el proceso Fenton se lleva a cabo a pH alrededor de tres. Los ensayos experimentales llevados a cabo en este trabajo estuvieron orientados a analizar la factibilidad de obtener resultados favorables sin necesidad de ajustar el pH inicial, trabajando a pH 5, ya que las vinazas, en general, presentan estos valores de pH debido a las condiciones del proceso de fermentación. Esto representaría una ventaja, además de contribuir a la simplicidad y economía del proceso.
Para los ensayos de tratamiento de vinaza por oxidación se seleccionó la muestra con mayor valor de DQO Se realizaron cinco experiencias con 20 mL de vinaza y diferentes volúmenes de peróxido de hidrógeno (20 mL, 13 mL, 10 mL, 5 mL y 2.5 mL, respectivamente). Se dejó reaccionar y se tomaron muestras a 1 día, 2 días y 5 días. Estos ensayos se realizaron por duplicado.
Se calculó la relación de oxígeno (RO), relación entre la cantidad de oxígeno necesario para oxidar la vinaza inicial (DQO del efluente) y la cantidad de oxígeno que provee el peróxido de hidrógeno agregado en el ensayo (Ecuación 1):
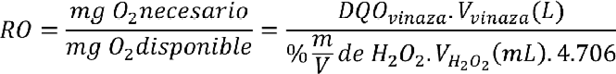 (E. 1)
(E. 1)
La vinaza es un efluente multicomponente, por ello que se consideró de manera global la cantidad de oxígeno necesaria para oxidar todo lo susceptible de ser oxidable en cada momento del ensayo, con la medición de DQO de la mezcla reactiva. Este parámetro se usó para determinar la eficiencia del tratamiento.
En el Cuadro 1 se muestran los resultados obtenidos en las determinaciones fisicoquímicas de las cuatro vinazas analizadas, identificadas como L, F, C y S. Se puede observar el valor calculado del IB.
Cuadro 1. Caracterización fisicoquímica de vinazas generadas en destilerías de la provincia de Tucumán.
Table 1. Physical-chemical characterization of vinasse generated in distilleries in the province of Tucuman.
|
Parámetro |
Método |
Unidades |
Vinaza L |
Vinaza F |
Vinaza C |
Vinaza S |
|
pH |
SM4500H-B |
u. de pH |
5.1 |
5.5 |
6.1 |
5.2 |
|
Conductividad |
SM2510 |
mS.cm-1 |
42.0 |
44.5 |
46.1 |
28.7 |
|
DQO |
SM5220-D |
mg.L-1 |
82 951 |
76 224 |
67 414 |
90 800 |
|
DBO5 |
SM5210B |
mg.L-1 |
37 224 |
22 424 |
35 024 |
40 600 |
|
ST |
SM2540-E |
g.100 mL-1 |
9.8 |
7.1 |
6.0 |
10.8 |
|
SS (2 hrs) |
SM2540-F |
mL.L-1 |
67 |
56 |
45 |
74 |
|
Potasio |
SM3500K-D |
g.L-1 |
10.0 |
16.0 |
9.0 |
8.6 |
|
Cobre |
SM3500Cu-B |
mg.L-1 |
3.9 |
3.2 |
4.1 |
4.4 |
|
Zinc |
SM3500Zn-B |
mg.L-1 |
2.7 |
1.8 |
2.9 |
3.0 |
|
Hierro |
SM3500Fe-B |
mg.L-1 |
80 |
69 |
56 |
78 |
|
Índice de biodegradabilidad |
0.45 |
0.29 |
0.52 |
0.45 |
L, F, C y S: código de identificación de muestras de vinazas de diferentes destilerías; ST: sólidos totales; SS: sólidos sedimentables; DBO: demanda bioquímica de oxígeno; DQO: demanda química de oxígeno; SM: método estándar (APHA, 2005).
De acuerdo con el criterio de biodegradabilidad (Ardila et al., 2012), tres de las vinazas analizadas (L, S y C) resultaron poco biodegradables ya que el índice se encontró entre 0.30 y 0.70; mientras que la vinaza F se clasificó como no biodegradable (IB< 0.30).
Una relación DBO/DQO alrededor de 0.45, significa que contiene aproximadamente un 45 % de materia orgánica biodegradable y es un efluente en el que podría aplicarse un tratamiento biológico, aunque el elevado contenido de sales puede resultar desfavorable porque podría retardar el inicio de este. La vinaza F presentó un IB de 0.29, lo cual significa que contiene una elevada proporción de materia orgánica no biodegradable. Según Sánchez-Proaño y García-Gualoto (2018), efluentes con bajo IB, requieren la aplicación de tratamiento químico, previo al tratamiento biológico.
En general. las vinazas presentaron características ácidas y valores altos de conductividad eléctrica, hasta 46 mScm-1. La mayor parte de los sólidos totales corresponden a los sólidos totales volátiles de naturaleza orgánica. Los sólidos totales fijos corresponden a compuestos inorgánicos presentes en la vinaza. Estos factores, unidos a la acidez y a la temperatura a la cual se descargan las vinazas de destilerías, provocan su alto poder corrosivo (Ibarra-Camacho et al., 2019).
El potasio es el metal en mayor proporción, con valores de hasta 10 g.L-1, en tanto el hierro presenta valores considerables de hasta 80 mg.L-1. Se observa que estos valores se encuentran dentro del rango de los valores típicos (Zúñiga-Cerón y Gandini-Ayerbe, 2013).
En el Cuadro 2 se comparan los valores promedios de las vinazas analizadas y los valores máximos permitidos, según la Resol N.° 30 de la Secretaría de Medioambiente (SEMA) de la provincia de Tucumán, para descarga de efluentes en suelo y en cuerpos de agua superficial (naturales o artificiales), la deposición para absorción en suelo comprende pozos absorbentes, lagunas y riego. Los parámetros determinados en vinaza superan ampliamente los valores máximos permitidos por la normativa vigente; esto sumado al volumen del efluente generado por litro de etanol producido, hacen del mismo un residuo líquido altamente contaminante.
Cuadro 2. Valores promedios de parámetros fisicoquímicos analizados en vinaza y valores límites permitidos por la legislación provincial (Resol N.° 30 SEMA, 2009), para desacarga en agua y en suelo.
Table 2. Average values of physical-chemical parameters analyzed in vinasse and limit values allowed by provincial legislation, for discharge into water and soil.
|
Parámetro |
Unidades |
Promedio en vinazas |
Valores máximos (SEMA) |
|
|
agua |
suelo |
|||
|
pH |
5.5 ± 0.1 |
≥6 y £ 9 |
≥ 6 y ≤ 9 |
|
|
Conductividad |
mS.cm-1 |
40 200 ± 500 |
≤1000 |
No Establecido |
|
DQO |
mg.L-1 |
79 347± 1000 |
≤ 250 |
≤ 500 |
|
DBO5 |
mg.L-1 |
33 818 ± 500 |
≤ 50 |
≤ 250 |
|
S. S. (2 días) |
mg.L-1 |
60.5 ± 0.5 |
≤ 1 |
≤ 5 |
|
Cobre |
mg.L-1 |
3.9 ± 0.1 |
≤ 0.3 |
Ausente |
|
Zinc |
mg.L-1 |
2.6 ± 0.1 |
≤ 1 |
≤ 1 |
|
Hierro |
mg.L-1 |
70.8 ±0.1 |
≤ 2 |
≤ 0.1 |
SEMA: Secretaría de Medioambiente de la provincia de Tucumán, Argentina. DQO: demanda química de oxígeno; DBO5: demanda bioquímica de oxígeno en cinco días; SS.: sólidos sedimentables a los dos días.
La vinaza S presentó el mayor valor de DQO, por lo que se ensayó el tratamiento oxidativo por duplicado sobre una porción de esta. En la Figura 1 se muestra el aspecto de la masa reaccionante inicial y final, a los cinco días de reacción, en el ensayo con ٢٠ mL de vinaza S y 20 mL de peróxido de hidrógeno. Puede observarse el color marrón oscuro de la vinaza inicial; luego de un día de reacción se notó una disminución del color, efecto que se acentúa al transcurrir el tiempo, tal que a los cinco días se distingue una coloración amarillo claro y cierta turbidez, por la presencia de un precipitado blanco. Se decidió finalizar la reacción a los cinco días porque, en pruebas preliminares, entre 5 y 10 días, el valor de DQO se modificaba solo un 1 %.


Figura 1. Aspecto físico de la vinaza S inicial (foto izquierda) y posterior al tratamiento (foto derecha) con peroxido de hidrógeno, luego de 5 días de reacción. Ensayo con Relación de Oxígeno (RO) igual a 1.
Figure 1. Physical aspect of the initial vinasse S (left photo) and after treatment (right photo) with hydrogen peroxide, after 5 days of reaction. Test with Oxygen Ratio (OR) equal to 1.
En el Cuadro 3 se muestran los resultados obtenidos en los 5 ensayos realizados con vinaza S y diferentes RO; es decir, con distinta relación de oxígeno necesario y disponible. Los valores de DQO corresponden al promedio de los ensayos duplicados.
Se observa una disminución de los valores de DQO, en todos los casos, obteniéndose el menor valor en el ensayo 4. En los ensayos 1, 2 y 3, con una RO mayor que 1, se obtuvieron valores de DQO final (5 días) que resultaron ser mayores que en el caso de RO igual a 1 (ensayo 4). Esto significa que la cantidad de peróxido de hidrógeno (la cual provee el oxígeno disponible) se encontraba en defecto respecto de la demanda de oxígeno, por lo que la oxidación de materia orgánica se produjo hasta que este se consume, llegando a un valor de DQO remanente mayor, a menor volumen de peróxido de hidrógeno usado, comparando siempre a los 5 días de reacción. Claramente el peróxido de hidrógeno fue el reactivo limitante.
Cuadro 3. Variación de demanda química de oxígeno (DQO) en función del tiempo de reacción (días). Oxidación de 20 mL de vinaza S con diferentes volúmenes de oxidante.
Table 3. Variation of chemical oxygen demand (COD) as a function of time (days). Oxidation reaction of 20 mL of vinasse S with different volumes of oxidant.
|
Volumen de H2O2 (mL) |
RO |
DQO inicial (mg/L) |
DQO-Día 1 (mg/L) |
DQO-Día 2 (mg/L) |
DQO-Día 5 (mg/L) |
|
|
ENSAYO 1 |
2.5 |
5.5 |
89 878 |
82 951 |
76 224 |
64 410 |
|
ENSAYO 2 |
5.0 |
2.7 |
89 140 |
77 625 |
65 000 |
40 000 |
|
ENSAYO 3 |
10.0 |
1.4 |
88 033 |
70 794 |
50 000 |
22 000 |
|
ENSAYO 4 |
13.0 |
1.0 |
87 530 |
63 096 |
40 000 |
14 000 |
|
ENSAYO 5 |
20.0 |
0.7 |
86 650 |
60 132 |
48 000 |
35 500 |
RO: relación de oxígeno: mg de oxígeno necesario (expresado como DQO)/mg de oxígeno aportado por peróxido de hidrógeno.
En el ensayo 5, que se llevó a cabo con 20 mL de peróxido de hidrógeno, la cantidad de oxígeno disponible para la oxidación fue mayor que la cantidad de oxígeno necesario (RO< 1); es decir, se suministró oxidante en exceso. En este caso se obtuvo una disminución de DQO del 60 %, lo cual lleva a pensar que el exceso de oxidante fue contraproducente en las condiciones en las que se realizó el ensayo.
Se calculó el porcentaje de remoción de DQO (relación entre la disminución de DQO respecto del valor inicial, luego de 5 días de reacción). Obsérvese, en la Figura 2, que la mayor remoción de DQO (85 %) se logró cuando se empleó un volumen de peróxido de hidrógeno tal que la RO sea 1; es decir, la cantidad estequiométrica de oxígeno necesario para la oxidación de 20 mL de vinaza S con DQO de 90 800 mg/L.
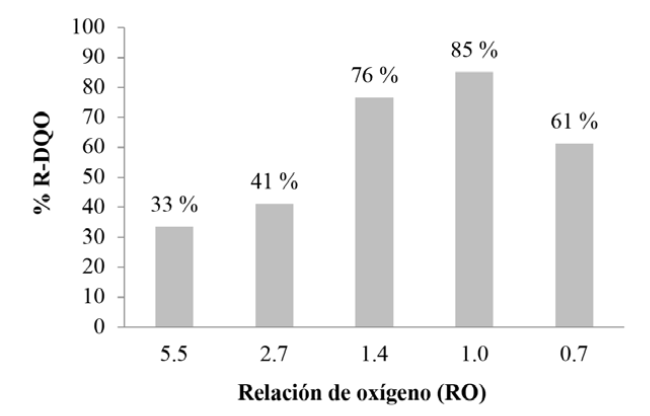
Figura 2. Porcentaje de remoción de DQO en vinaza S tratadas con peróxido de hidrógeno, para diferente relación de oxígeno (RO), luego de 5 días de reacción.
Figure 2. Percentage of COD removal in vinasse S treated with hydrogen peroxide, for different oxygen ratio (RO), after 5 days of reaction.
Se podría afirmar que la destrucción de la carga contaminante se llevó a cabo por reacciones de oxidación del tipo Fenton, con generación de radicales hidroxilos, catalizada por el elevado contenido de iones metálicos, Fe2+ y Cu2+ como componentes naturales de las vinazas.
La reacción de Fenton es uno de los métodos de oxidación avanzada que se ha aplicado ampliamente para el tratamiento de aguas residuales que contienen contaminantes orgánicos (Pimentel-Prates et al., 2023). Se publicaron trabajos científicos, a nivel experimental, donde se usó el proceso Fenton para el tratamiento de vinazas de caña de azúcar, trabajando a pH 3.8 y exceso de peróxido de hidrógeno, logrando reducción de DQO del 48 % y un aumento en la biodegradabilidad, en un tiempo de 60 minutos (Hakika et al., 2019). En otros casos, se aplicó Fenton en forma conjunta con otro tratamiento para lograr resultados más eficientes en la destrucción de la materia orgánica. Guerreiro et al. (2016) combinaron el proceso Fenton con coagulación y floculación, con reducción de DQO de hasta un 69.2 %. Por su parte, Campos-Díaz et al. (2017) trabajaron con el tratamiento de la vinaza sin diluir mediante un proceso biológico y un proceso de oxidación avanzada, ambos acoplados secuencialmente; así, en el tratamiento biológico se realizó en un bioreactor de lecho fluidizado inverso con un consorcio microbiano utilizando polipropileno como material de soporte; luego, la vinaza se alimentó de forma continua a un fotoreactor donde se llevó a cabo la reacción Fenton fotoasistida con UV; los resultados mostraron la eliminación total de DQO (99 %) en un tiempo de 90 días. Se investigó el uso de una especie de hongo, seguido de la oxidación electroquímica para la degradación de la vinaza de caña de azúcar, alcanzando una remoción de color final del 100 % y DQO de 66 % (Vilar et al., 2018).
En el ensayo 5, la menor disminución de DQO con exceso de oxidante coincide con los resultados obtenidos en otros estudios (Ahmadi et al., 2015; Alnaizy y Akgerman, 2000), los cuales informan que el exceso en la aplicación de peróxido de hidrógeno y las altas concentraciones de radicales OH• originan reacciones competitivas que producen efectos inhibitorios en la degradación de materia orgánica, pues el peróxido de hidrógeno actúa capturando radicales hidroxilos.
El proceso Fenton requiere pH ácido, siendo una de las principales desventajas, pues en la mayoría de los efluentes se requiere la adición de ácido para ajustar el pH y agregado de bases para neutralización al final del tratamiento. A pH > 4 la generación de radicales hidroxilos es inhibida por la formación de precipitado de hidróxido férrico (Hakika et al., 2019). En el presente estudio, sin embargo, durante los ensayos de oxidación de vinazas, el pH se mantuvo cercano a 5 y no se observó la presencia del precipitado de hidróxido férrico. Chiva-Vicent et al. (2017) realizaron una revisión de investigaciones en las que se usaron modificaciones del reactivo de Fenton para permitir su aplicación a condiciones de pH menos rigurosas. Los autores afirman que la presencia de otros metales catalizadores, como cobre y manganeso, participan en la generación de radicales hidroxilos, a pH 5. También las sustancias húmicas permiten la aplicación oxidación con peróxido de hidrógeno a pH entre 5 y 8, ya que contienen grupos funcionales capaces de formar complejos solubles con hierro, lo cual evitar su precipitación (Mikutta y Kretzschmar, 2011).
Las vinazas tratadas con peróxido de hidrógeno aún superan los valores máximos permitidos indicados por la normativa vigente (Resolución N.° 30/09-SEMA) para efluentes industriales descargados en agua superficial (250 mg/L) y para absorción en suelo (500 mg/L). A pesar de esto, es evidente que la DQO de la mezcla final es mucho menor que la inicial de la vinaza, y la diminución porcentual es importante.
Esta mejora se manifestó también con el aumento del IB Al finalizar el ensayo de tratamiento de vinaza con RO de 1, el valor de DBO promedio fue de 8 560 mg/L, con lo cual se calculó el IB final de 0.61. Teniendo en cuenta que la vinaza inicial presentó un valor de IB de 0.45, se observó una mejora sustancial en la calidad del efluente. Estos resultados están de acuerdo con lo reportado por Hakika et al. (2019), quienes reportan que el proceso oxidativo mejora las características biodegradables de efluentes, por lo que podría usarse como tratamiento previo al tratamiento biológico.
Los mejores resultados se obtuvieron cuando la relación entre el oxígeno necesario para la oxidación y el aportado por el oxidante fue igual a 1. Esto significa que la demanda química de oxígeno del efluente debería ser igual a la cantidad de oxígeno suministrado por el peróxido de hidrógeno. De la Ecuación 1 se despeja el volume de oxidante:
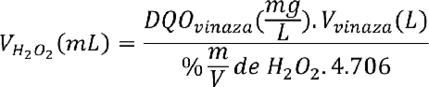 (E. 2)
(E. 2)
La Ecuación 2 representa la expresión matemática que permite calcular el volumen de peróxido de hidrógeno requerido para la oxidación de vinazas, en función del valor de DQO inicial del efluente. Esto es importante porque la vinaza producida como residuo en la obtención de etanol por fermentación puede presentar valores diferentes de DQO, dependiendo de las características del mosto fermentado, de la eficiencia de la destilación y de la región de donde proviene la materia prima. En general, todas las vinazas presentan elevados contenidos de hierro, cobre, manganeso y ácidos húmicos, que, como se mencionó anteriormente, favorecen la reacción de oxidación.
El avance de la reacción de oxidación se siguió con la medición de DQO, es decir, determina la concentración de las sustancias que permanecen sin oxidar, en cada tiempo, como los mg de oxígeno necesarios para oxidar los componentes oxidables. Esto permite expresar la velocidad de la reacción global como se muestra en la Ecuación 3.
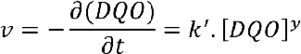 (E. 3)
(E. 3)
Siendo , el orden de la reacción; , constante aparente de proporcionalidad que contiene a la constante de velocidad específica a 30 °C; representa la velocidad de consumo de oxígeno por las sustancias oxidables y , el tiempo en días.
Asumiendo que se trata de una reacción de primer orden respecto de DQO, la expresión integrada sería: ln DQOf= ln DQOi – k`.t. En la Figura 3 se muestra la gráfica de lnDQO = f(t), para los datos obtenidos con RO=1, que correspondería al caso de mayor remoción de DQO. Se observa que los valores ajustan a una recta cuya ecuación se muestra en la gráfica (Figura 3). El coeficiente de determinación (R2) es 0.998, por lo que se puede afirmar que los datos experimentales responden al modelo lineal propuesto.
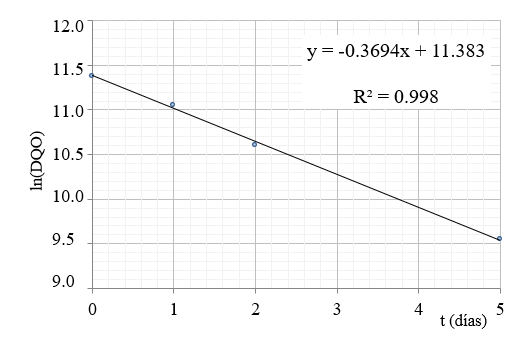
Figura 3. Verificación de cinética de la reacción de oxidación de vinaza con peróxido de hidrógeno. Reacción de primer orden respecto de DQO.
Figure 3. Verification of kinetics of the reaction of vinasse oxidation with hydrogen peroxide. 1° order reaction with respect to COD.
En consecuencia, se puede afirmar que la degradación de vinaza por proceso oxidativo, con peróxido de hidrógeno, responde a una cinética de primer orden respecto de DQO, con un valor de k’ aparente de 0.3694 (L/mg.día).
La velocidad de la reacción es relativamente baja, pero en 5 días se logra una disminución importante de DQO, con un proceso relativamente económico, donde el único reactivo que se emplea es el peróxido de hidrógeno. Se publicaron numerosos trabajos de investigación donde se estudia la destrucción de contaminantes con procesos oxidativos comprobando una cinética de primer orden o pseudoprimer orden, como ser la degradación del ftalato de dietilo (DEP) por oxidación Fenton homogénea y heterogénea, con diferentes fuentes de hierro (Bensalah et al., 2019); la degradación de ácido oxálico en efluentes líquidos de una planta nuclear, por reacción foto-Fenton (Kim et al., 2019); la destrucción de hidrocarburos policíclicos aromáticos en agua por foto-Fenton (Abd-Manan et al., 2019) y eliminación de antibióticos mediante fotoreactor solar Fenton (Bensaibi et al., 2023).
En los estudios mencionados, los procesos que incluyen reacciones Fenton suelen ser más rápidos, con valores de constantes de velocidad más elevados, pero las condiciones fueron diferentes a las del presente estudio, pues se llevaron a cabo a pH entre 2 y 3, con cantidades óptimas de catalizador ferroso (mol Fe2+ = 1/16 mol H2O2). Sin embargo, los resultados logrados con el tratamiento propuestos son prometedores, porque requiere menor tiempo que los tratamientos biológicos que actualmente se aplican, donde en general el tiempo de residencia llega hasta 35 días.
El tratamiento de vinazas usando proceso oxidativo con peróxido de hidrógeno, produce disminución de DQO del efluente, disminución de color y aumento de transparencia. Se cree que se trata de una reacción de oxidación catalizada por iones Fe2+ y Cu2+ contenidos en el efluente, cuya naturaleza ácida permite la remoción de DQO a pH 5, favorecido por la presencia de ácidos húmicos.
Los ensayos experimentales permitieron afirmar que los mejores resultados, en condiciones ambientales, se lograron con cantidades estequiométricas de oxidante peroxido de hidrógeno, teniendo en cuenta el valor de DQO inicial del efluente, lográndose una disminución de DQO del 85 %, con una cinética de primer orden.
Con el tratamiento propuesto, se consiguió aumentar el Índice de Biodegradabilidad, por lo que podría aplicarse como tratamiento químico, previo al tratamiento biológico, y mejoraría la eficiencia de este último.
Este proceso es aplicable, solo emplea peróxido de hidrógeno como reactivo adicional y se lleva a cabo en condiciones ambientales, por lo que se recomienda continuar los estudios tendientes a lograr su aplicación a mayor escala, de manera que represente una opción viable para responder al desafío ambiental que representan las vinazas en América Latina.
5.Ética y conflicto de intereses
Las autoras declaran que han cumplido con todos los requisitos éticos y legales pertinentes, tanto durante el estudio como en la producción del manuscrito; que no hay conflictos de intereses de ningún tipo; que todas las fuentes financieras se mencionan completa y claramente en la sección de agradecimientos; y que están de acuerdo con la versión final editada del artículo.
Se agradece a la Universidad Nacional de Tucumán, a través de la Secretaría Ciencia, Arte e Innovación Tecnológica (SCAIT), por el aporte económico realizado al proyecto PIUNT E710, “Propiedades Fisicoquímicas de mezclas. Tratamiento Oxidativo de Efluentes Industriales. Vinazas. Agroquímicos”, en el marco del cual se llevó a cabo el presente trabajo. También agradecemos al equipo editorial de la revista y a las personas revisoras anónimas por sus observaciones a la versión final del escrito.
Abd-Manan, T.; Khan, T.; Sivapalan, S.; Jusoh, H.; Sapari, N.; Sarwono, A.; Mahirah- Ramli, R.; Harimurti, S.; Beddu, S.; Nabihah-Sadon, S.; Mohd-Kamal, L. y Malakahmad, A. (2019). Application of response surface methodology for the optimization of polycyclic aromatic hydrocarbons degradation from potable water using photo-Fenton oxidation process. Science of The Total Environment, 665, 196-212. https://doi.org/10.1016/j.scitotenv.2019.02.060
Ahmadi, M.; Ramavandi, B. y Sahebi, S. (2015). Efficient degradation of a biorecalcitrant pollutant from wastewater using a fluidized catalyst-bed reactor. Chemical Engineering Communications, 202, 1118-1129. http://dx.doi.org/10.1080/00986445.2014.907567
Ahmed, O.; Sulieman, A. y Elhardallou, S. (2013). Physicochemical, chemical and microbiological characteristics of vinasse, a by-product from ethanol industry. American Journal of Biochemistry, 3(3), 80-83. http://article.sapub.org/10.5923.j.ajb.20130303.03.html
Alnaizy, R. y Akgerman, A. (2000). Advanced Oxidation of Phenolic Compounds. Advances in Environmental Research, 4, 233-244. https://doi.org/10.1016/S1093-0191(00)00024-1
APHA, AWWA WEF (2005). Standard Methods for the Examination of Water and Wastewaters. 21 th edition. USA.
Ardila, A.; Reyes Calle, J; Arriola-Villaseñor, E. y Hernández, J. (2012). Remoción fotocatalítica de DQO, DBO5 y COT de efluentes de la industria farmacéutica. Revista Politécnica, 8 (15), 9-17. https://revistas.elpoli.edu.co/index.php/pol/article/view/316
Bensaibi, F.; Chabani, M.; Bouafia, S. y Djelal, H. (2023) Doxycycline Removal by Solar Photo-Fenton on a Pilot-Scale Composite Parabolic Collector (CPC) Reactor. Processes, 11, 2363. https://doi.org/10.3390/pr11082363
Bensalah, N.; Dbira, S. y Bedoui, A. (2019). Mechanistic and kinetic studies of the degradation of diethyl phthalate (DEP) by homogeneous and heterogeneous Fenton oxidation. Environmental Nanotechnology, Monitoring & Management, 11. https://doi.org/10.1016/j.enmm.2019.100224
Bermúdez, R.; Hoyos, J. y Rodríguez, S. (2000). Evaluación de la disminución de la carga contaminante de la vinaza de destilería por ensayo anaeróbico. Revista Internacional de Contaminación Ambiental, 16, 103-107. https://www.redalyc.org/articulo.oa?id=37016302
Cabrera, A. (2013). Tratamiento de vinazas en un filtro anaerobio empacado de flujo ascendente. Tesis en opción al grado de Máster en Ingeniería Ambiental, ISPJAE, La Habana, Cuba.
Campos-Díaz, K.; Álvarez-Cruz, J.; Lira-Rodríguez, M. y Bandala, E. (2017). Coupled Inverse Fluidized Bed Bioreactor with Advanced Oxidation Processes for Treatment of Vinasse. AIMS Geosciences, 3(4), 538-551. https://www.aimspress.com/article/doi/10.3934/geosci.2017.4.538
Centro Azucarero Argentino. (2021). Estadísticas-Producción de alcohol. https://centroazucarero.com.ar/produccion-de-alcohol-2020-2029/
Chanfón-Curbelo, J. y Lorenzo-Acosta, Y. (2014). Alternativas de Tratamiento de las Vinazas de Destilería. Experiencias Nacionales e Internacionales. Centro Azúcar, 41(2), 56-67. http://centroazucar.uclv.edu.cu/media/articulos/PDF/2014/2/6.pdf
Chiva-Vicent, S.; Berlanga-Clavijo, J.; Martinez-Cuenca, R. y Climent, A. (2017). Procesos de oxidación avanzada en el ciclo integral del agua. En Chiva-Vicent, S. (Ed). Castello de la Plana: Publicacions de la Universitat Jaume I, D. L. http://dx.doi.org/10.6035/UJI.FACSA.2017.1
Christofoletti, C.; Escher, J.; Correia, J.; Urbano Marinho, J. y Fontanetti, C. (2013). Sugarcane vinasse: Environmental implications of its use. Waste Management, 33, 2752-2761. https://www.sciencedirect.com/science/article/abs/pii/S0956053X1300408X
Collins, J. y Bolton, J. (2016) Advanced Oxidation Handbook. EE. UU.: American Water Works Association.
de la Cruz, S. (2002). Aplicaciones del análisis complejo de procesos en el estudio de alternativas de integración de un complejo agroindustrial azucarero con una planta de alcohol. Tesis presentada para la opción del Grado Científico de Doctor en Ciencias Técnicas. Universidad Central de Las Villas, Santa Clara, Cuba.
Domenech, X.; Jardim Wilson, F. y Litter, I. (2001). Procesos avanzados de oxidación para la eliminación de contaminantes. https://www.academia.edu/14116027/PROCESOS_AVANZADOS_DE_OXIDACI%C3%93N_PARA_LA_ELIMINACI%C3%93N_DE_CONTAMINANTES. (Accedido el 10/11/2021)
España-Gamboa, E.; Mijangos-Cortes, J.; Barahona-Perez, L.; Dominguez-Maldonado, J.; Hernádez-Zarate, G. y Alzate-Gaviria, L. (2011). Vinasses: characterization and treatments. Waste Management & Research, 29(12), 1235-1250.
Fenton, H. (1894). Journal of the Chemical Society, 65, 899-910.
García-Gámez, C., Gortáres-Moroyoqui, P. y Drogui, P. (2011). Tratamientos Biológicos y de oxidación avanzada combinados para una solución a la biotecnología Ambiental. Ide@s CONCYTEG, 6(71), 585-605.
Guerreiro, L.; Rodrigues, C.; Duda, R.; de Oliveira, R.; Boaventura, R. y Madeira, L. (2016). Treatment of sugarcane vinasse by combination of coagulation/flocculation and Fenton’s oxidation. Journal of Environmental Management, 181, 237-248.
Hakika, D.; Sarto, S.; Mindaryani, A. y Hidayat, M. (2019). Decreasing COD in Sugarcane Vinasse Using the Fenton Reaction: The Effect of Processing Parameters. Catalysts, 9(11), 881. http://dx.doi.org/10.3390/catal9110881
Ibarra-Camacho, R.; León- Duharte, L. y Osoria-Leyva, A. (2019). Caracterización fisico-química de vinazas de destilerias. Revista Cubana de Química, 31(2), 246-257. http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S2224-54212019000200246&lng=es&tlng=es
Jiang, Z.; Li, Y.; Wei, G.; Liao, Q.; Su, T.; Meng, Y.; Zhang, H. y Lu, C. 2012. Effect of long-term vinasse application on physico-chemical properties of sugarcane field soils. Sugar Technology, 14, 412-417.
Kim, J.; Lee, H.; Park, Y.; Lee, S.; Choi, S.; Oh, W.; Kim, H.; Kim, C.; Kim, K. y Seo, B. (2019). Studies on decomposition behavior of oxalic acid waste by UVC photo-Fenton advanced oxidation process. Nuclear Engineering and Technology, 51(8), 1957-1963. https://doi.org/10.1016/j.net.2019.06.011
Laime, E.; Fernandes, P.; Oliveira, D. y Freire, E. (2011). Possibilidades tecnológicas para a destinação da vinhaça: uma revisão. Revista Trópica: Ciencias Agrárias e Biológicas, 5, 16-29.
Ley 26 093 Régimen de Regulación y Promoción para la Producción y Uso Sustentables de Biocombustibles. (2006). http://www2.congreso.gob.pe/sicr/cendocbib/con4_uibd.nsf/ 543D E964A4D8659005257CC300776133/$FILE/Ley_26093.pdf.
Lim, S.; Lee, L. y Wu, T. (2016). Sustainability of using composting and vermicomposting technologies for organic solid waste biotransformation: Recent overview, greenhouse gases emissions and economic analysis. Journal of Cleaner Production, 111, 262-278. https://doi.org/10.1016/j.jclepro.2015.08.083
Litter, M. y Slodowicz, M. (2017). An overview on heterogeneous Fenton and photo Fenton reactions using zerovalent iron materials. Journal of Advanced Oxidation Technologies, 20(1). https://doi.org/10.1515/jaots-2016-0164
Mikutta, C. y Kretzschmar, R. (2011). Spectroscopic evidence for ternary complex formation between arsenate and ferric iron complexes of humic substances. Environmental Science and Technology, 45, 9550-9557. https://doi.org/10.1021/es202300w
Ospina-León, L.; Manotas-Duque, D. y Ramírez-Malule, H. (2023). Desafíos y oportunidades de la Vinaza de caña de azúcar. Un análisis bibliométrico. Ingeniería y competitividad, 25(1), e-30412144. https://doi.org/10.25100/iyc.v25i1.12144
Pérez-Bermúdez, I. y Garrido-Carraler, N. (2006). Aprovechamiento integral de vinazas de destilerías. Una revisión actual. Revista Ingeniería Química, 129-133.
Pimentel Prates, M.; de Oliveira Loures Marcionílio, S. M.; Borges Machado, K.; Medeiros de Araújo, D.; Martínez-Huitle, C. A.; León Arantes, A. L. y Ferreira da Silva Gadêlha, J. E. (2023). Fenton: una revisión sistemática de su aplicación en el tratamiento de aguas residuales. Procesos, 11, 2466. https://doi.org/10.3390/pr11082466.
Poyatos J.; Muñio M.; Almecija, M.; Torres, J.; Hontoria, E. y Osorio F. (2010). Advanced oxidation processes for wastewater treatment: state of the art. Water, Air, Soil Pollution, 205, 187-204. https://doi.org/10.1007/s11270-009-0065-1
Secretaría de Estado de Medio Ambiente (SEMA) de la provincia de Tucumán. (2009). Resolución N.° 30. http://www.sematucuman.gob.ar/web/index.php/31-normativa/idga/idga pngclosrechidricos/153-iga-pgrh-resolucion030-sema
Ministerio de Energía y Minería. (2016). Resolución 37/2016. Boletín Oficial de la República Argentina. https://www.boletinoficial.gob.ar/pdf/linkQR/cVUvOEdIcEZTdGMrdTVRe Eh2ZkU0dz09
Robles-González, V.; Galindez-Mayer, J.; Rinderknecht-Seijas, N. y Poggi-Varaldo, H. (2012). Treatment of mezcal vinasses: A review. Journal of Biotechnology, 157(4), 524-546. https://doi.org/10.1016/j.jbiotec.2011.09.006
Sánchez-Proaño, R. y García-Gualoto, K. (2018). Tratamiento de aguas residuales de cargas industriales con oxidación avanzada en sistemas convencionales. LA GRANJA: Revista de Ciencias de la Vida, 27(1), 103-111.
Sangave, P.; Gogate, P. y Pandit, A. (2007). Combination of ozonation with conventional aerobic oxidation for distillery wastewater treatment. Chemosphere, 68(1), 32-41. https://doi.org/10.1016/j.chemosphere.2006.12.053
Sanz, J.; Lombraña, J. y de Luis, A. (2013). Estado del Arte en la Oxidación Avanzada a Efluentes Industriales: Nuevos Desarrollos y Futuras Tendencias. Afinidad LXX, 561. https://www.raco.cat/index.php/afinidad/article/download/268536/356125
Satyawali, Y. y Balakrishnan M. (2008). Wastewater treatment in molasses-based alcohol distilleries for COD and color removal: A review. Environmental Management, 86, 481-497. https://doi.org/10.1016/j.jenvman.2006.12.024
Sim, E. y Wu, T. (2010). The potential reuse of biodegradable municipal solid wastes (MSW) as feedstocks in vermicomposting. Journal of the Science of Food and Agriculture, 90(13), 2153-2162. https://doi.org/10.1002/jsfa.4127
Stefan, M. (ed.). (2017). Advanced Oxidation Processes for Water Treatment: Fundamentals and Applications. Londres: EWA Publishing.
Valeiro, A. y Portocarrero, R. (2017). Gestión de las vinazas sucro-alcoholeras en Brasil. Serie: Gestión de residuos de la industria sucro-energética argentina. INTA Ediciones.
Vilar, D.; Carvalho, G.; Pupo, M.; Aguiar, M.; Torres, N.; Américo, J.; Cavalcanti, E.; Eguiluz, K.; Salazar Banda, G.; Leite, M. y Ferreira, L. (2018). Vinasse degradation using Pleurotus sajor-caju in a combined biological-Electrochemical oxidation treatment. Separation and Purification Technology, 192: 287-296. https://www.sciencedirect.com/science/article/pii/S1383586617315757
Zúñiga-Cerón, V. y Gandini-Ayerbe, M. (2013). Caracterización Ambiental de las Vinazas de Residuos de Caña de Azúcar Resultantes de la Producción de Etanol. DYNA, 80(177), 124-131. https://www.redalyc.org/articulo.oa?id=49625661016
1 Especialista en Ciencias Exactas e Ingeniería, profesora asociada, química general de la Facultad de Ciencias Exactas y Tecnología de la Universidad Nacional de Tucumán, Tucumán, Argentina. achaile@herrera.unt.edu.ar; https://orcid.org/0000-0001-8070-2413
2 Ingeniera Química, jefe de Trabajos Prácticos, Facultad de Ciencias Exactas y Tecnología, Universidad Nacional de Tucumán, Tucumán, Argentina. meuboldi@herrera.unt.edu.ar; https://orcid.org/0000-0003-1831-086X
3 Especialista en ingeniería, profesora, Facultad Regional Tucumán, Universidad Tecnológica Nacional, Tucumán, Argentina. eferreyra@herrera.unt.edu.ar; https://orcid.org/0000-0001-6504-1020
Escuela de Ciencias Ambientales,
Universidad Nacional, Campus Omar Dengo
Apartado postal: 86-3000. Heredia, Costa Rica
Teléfono: +506 2277-3688
Correo electrónico revista.ambientales@una.ac.cr



