e-ISSN: 2215-3896.
(Enero-Junio, 2025). Vol 59 (1)
DOI: https://doi.org/10.15359/rca.59-1.7
Open Acces: www.revistas.una.ac.cr/ambientales
e-Mail: revista.ambientales@una.cr
Licencia: CC BY NC SA 4.0
Remoción de cromo (VI) de agua residual de curtiembre empleando biomasa orgánica vegetal en un reactor biológico secuencial aerobio
Removal of chromium (VI) from tannery wastewater using vegetable organic biomass in an aerobic sequential biological reactor
Alex Orestes Camacllanqui Huamanlazo1
[Recibido: 11 de marzo 2024, Aceptado: 13 de junio 2024, Corregido: 23 de julio 2024, Publicado: 9 de octubre 2024]
Resumen
[Introducción]: En la remoción de cromo (VI) de aguas residuales de curtiembre, los métodos fisicoquímicos son los más empleados. Sin embargo, estos demandan altos costos operativos y, peor aún, generan contaminantes secundarios que nuevamente requieren tratamientos complementarios para su eliminación. Ante ello, la aplicabilidad de la biomasa orgánica vegetal (BOV) emerge como una alternativa ambiental sobre la base de: la simplicidad de su obtención, la disminución como residuo, no genera contaminantes secundarios y, sobre todo, de remover cromo (VI). [Objetivo]: Usar residuos de BOV en un reactor biológico secuencial (RBS) aerobio, para la remoción de cromo (VI) en el tratamiento de agua residual de curtiembre. [Metodología]: Se implementaron 3 sistemas RBS aerobios; 2 controles (RBS1 y RBS2) y 1 materia de estudio (RBS+BOV). Cada sistema fue alimentado con agua residual de curtiembre (18 L) y conectado a un mecanismo de aireación (12.7 L/ min). El inóculo bacteriano, parte fundamental de un sistema RBS, se obtuvo a partir del cultivo selectivo de bacterias reductoras de cromo (VI) (BRCrVI), tomadas del agua residual en estudio e integradas al RBS2 y RBS+BOV a 0.6 g/L. La BOV se obtuvo de residuos de Stenotaphrum secundatum, fragmentado, tamizado, esterilizado e integrado al RBS+BOV a 1.5 g/L. [Resultados]: El sistema SRB+BOV alcanzó el mayor porcentaje de remoción de cromo (VI) (93 %), seguido por SBR2 (80.1 %) y, por último, de RBS1 (2.8 %). Con respecto a la DQO y SST, la prueba estadística (Tukey) arrojó que no había diferencia significativa entre el sistema en estudio y los controles, por lo que registró porcentajes de remoción de DQO que van de 87.8 % a 88.4 % y SST que van de 63.8 % a 69.2 %. [Conclusiones]: Se ha evidenciado la viabilidad del aprovechamiento de residuos de BOV para remover cromo (VI) en el tratamiento de agua residual de curtiembre. Los resultados de la presente investigación crean un panorama prometedor para mitigar los efectos derivados de la inadecuada gestión de las aguas residuales de curtiembre y de los residuos sólidos orgánicos.
Palabras clave: agua residual de curtiembre; biomasa orgánica vegetal (BOV); cromo (VI); reactor biológico secuencial (RBS) aerobio.
Abstract
[Introduction]: In the removal of chromium (VI) from tannery wastewater, physicochemical methods are the most used. However, these require high operating costs, and worse still, generate secondary pollutants that again require complementary treatments for their elimination. Given this, the applicability of vegetable organic biomass (VOB) emerges as an environmental alternative based on: the simplicity of its obtaining, the reduction as waste, it does not generate secondary pollutants and, above all, it removes chromium (VI). [Objective]: Use VOB waste in an aerobic sequential biological reactor (SBR) for the removal of chromium (VI) in the treatment of tannery wastewater. [Methodology]: 3 aerobic SBR systems were implemented; 2 controls (SBR1 and SBR2) and 1 study subject (SBR+VOB). Each system was fed with tannery wastewater (18 L) and connected to an aeration mechanism (12.7 L/min). The bacterial inoculum, a fundamental part of an SBR system, was gained from the selective culture of chromium (VI) reducing bacteria (RBCrVI) taken from the wastewater under study, and integrated into SBR2 and SBR+VOB at 0.6 g/L. The VOB was obtained from Stenotaphrum secundatum residues, fragmented, sieved, sterilized and integrated into the SBR+VOB at 1.5 g/L. [Results]: The SBR+VOB system achieved the highest percentage of chromium (VI) removal (93 %), followed by SBR2 (80.1 %), and finally SBR1 (2.8 %). With respect to COD and TSS, the statistical test (Tukey) showed that there was no significant difference between the system under study and the controls, recording COD removal percentages ranging from 87.8 % to 88.4 %, and TSS ranging from 63.8 % to 69.2 %. [Conclusions]: The viability of using VOB waste to remove chromium (VI) in the treatment of tannery wastewater has been evidenced. The results of this research create a promising panorama to mitigate the effects derived from inadequate management of tannery wastewater and organic solid waste.
Keywords: aerobic biological sequential reactor (SBR); chromium (VI); tannery wastewater; vegetable organic biomass (VOB).
La curtiembre resalta por ser una de las industrias que contribuye económicamente en los ingresos de una nación. Sin embargo, en países donde existe la ausencia del incumplimiento de normativas ambientales, dicha industria es catalogada como una de las que mayor impacto ambiental produce a causa de las aguas residuales que genera (Cortes & Martínez, 2017; Alam et al., 2020). En el Perú, al cierre del 2013, se estimó que había 92 empresas de curtiembre, ubicadas en 3 de las ciudades (Trujillo, Arequipa, Lima) donde existe un mayor desarrollo de esta industria (HELIANTHUS SAC, 2013, citado por Córdova et al., 2014). Esas ciudades no son ajenas al impacto ambiental generado por el vertimiento de las aguas residuales de esta industria y un claro ejemplo de ello son las empresas de curtiembre ubicadas en la cuenca del río Huaycolo-Lima, las identificadas en Trujillo-Libertad y las del Parque Industrial de Río Seco (PIRS) Cerro Colorado-Arequipa, que vierten sus aguas residuales sin ningún tratamiento a las alcantarillas; a pozas de oxidación constituidas solo para aguas servidas domiciliarias; a lagunas de oxidación colapsadas; en algunas ocasiones, directamente al río Huaycoloro, y, en casos particulares, son usadas para el riego de cultivos comestibles. En todos los escenarios, representan un riesgo ambiental relevante (Muñiz, 2016; Sánchez, 2018). Las curtiembres en el Perú, en general, usan sales de cromo como elemento curtiente para la piel. Este último logra retener, en promedio, del 60 al 80 % y lo restante se elimina como cromo total con el agua utilizada para la curtición (Córdova et al., 2014). Según Solís (2020), para procesar 1 tonelada de piel se usa en promedio 15 m3 de agua, volumen que al término del proceso se transforma en efluente.
Las etapas que componen el proceso de curtiembre se resumen en 3: ribera (remojo, pelambre, descarnado, dividido), curtido (desencalado, purga, piquelado, curtido, rebajado, neutralizado y recurtido) y acabado (recorte, acabado y almacén) (Huiman, 2022). En general, las aguas residuales de curtiembre producidas en esas fases, se caracterizan por presentar altos contenidos de demanda química de oxígeno (DQO), demanda bioquímica de oxígeno (DBO), sólidos suspendidos totales (SST), conductividad eléctrica (CE), sulfuros, aceites, grasas, cromo (III) y cromo (VI) (Kumari et al., 2016; Sánchez, 2022). Este último, según Castillo & López (2018) y Najarro (2021), durante la caracterización de muestras de agua residual de curtiembre, se hallaron a concentraciones que van desde 0.024 mg/L a 3.4 mg/L. Estos valores son alarmantes, debido a lo tóxico que resulta el cromo (VI) para la flora y fauna, incluso es asociado a la generación de cáncer en personas (Kimbrought et al., 2010). Singh & Chowdhuri (2017), al exponer a la Drosophila melanogaster a cromo (VI), evidenciaron un efecto neurotóxico sobre las células cerebrales. Por otro lado, en aves, peces, mamíferos y anfibios, al estar expuestos a aguas residuales con presencia de cromo (VI), se observaron cambios conductuales, morfológicos y citogenéticos, así que se le consideró un metal pesado de alto riesgo ambiental (Ferreira et al., 2018).
Entre los métodos empleados para la eliminación de cromo (VI) en el tratamiento de aguas residuales de curtiembre, los fisicoquímicos, donde se utilizan agentes como sulfuro de hidrógeno (H2S), sulfato de hierro (FeSO4), metabisulfito de sodio (NaHSO3) y polisulfuro de calcio (CaS5) son los más empleados; y se prefieren por la eficiencia o rapidez con la que remueven el cromo (VI) (Jobby et al., 2018; Kerur et al., 2021). Sin embargo, se ha demostrado que la utilización de estos agentes químicos genera contaminantes secundarios, los cuales requieren tratamientos complementarios para aplacar los efectos negativos que representan para el ambiente (Kerur et al., 2021; Saxena et al., 2021). Además, según Jobby et al. (2018) y Monroy et al. (2021), la aplicación de dichos métodos demanda elevados presupuestos operacionales, por los costos que amerita la compra de los agentes químicos; ello conlleva un panorama en el que las empresas de curtiembre (pequeñas, medianas y, peor aún, las informales) dejan de lado el manejo de sus aguas residuales, por los eminentes precios que representa invertir en su tratamiento. En este contexto, vienen emergiendo las tecnologías consideradas verdes, correspondientes a la aplicación métodos que usan residuos orgánicos considerados desechos para la eliminación de cromo (VI) de aguas residuales industriales, hecho que evita generar, en el proceso, subproductos dañinos para el ambiente (Kalidhasan et al., 2016; Narayanasamy et al., 2022). Uno de esos métodos, el cual viene siendo materia de estudio, utiliza biomasa orgánica vegetal como medio de adsorción y eliminación del cromo (VI) (Jobby et al., 2018; Bayuo, 2021). Se ha investigado la función de la biomasa orgánica vegetal (BOV) como fuente de remoción de cromo (VI) a escala laboratorio, exponiéndola a soluciones sintéticas de cromo (VI) en forma de cromato de potasio (K2CrO4). Se encontró que la BOV cuenta con diferentes fracciones de ácidos húmicos (AH) responsables de reducir las concentraciones de cromo (VI) de forma independiente (Gu et al., 2003). Estos AH, mediante los grupos funcionales que los componen, eliminan al cromo (VI) con mecanismos de complejación, adsorción y reducción química (Zhang et al., 2017). Por su parte, Chen et al. (2011) determinó que la fragmentación de la BOV es relevante para lograr un mayor porcentaje de remoción de cromo (VI), ya que, a menor peso molecular de la BOV, existe una mayor cantidad de grupos funcionales de AH que están en contacto directo con el cromo (VI), facilitando, en mayor medida, la eficiencia de remoción de cromo (VI).
Por otra parte, los estudios realizados por Singh & Srivastava (2010), Farabegoli et al. (2004) y Durai et al. (2011) resaltan la aplicabilidad de los reactores biológicos secuenciales (RBS) aerobios en el tratamiento de aguas residuales industriales, ya que eliminan parámetros como DQO, DBO, N, P, C, SST, por medio de microorganismos y aireación. Además, son considerados ambientalmente eficientes, de bajo costo y fácil operación.
Tomando como base lo manifestado, el objetivo de la presente investigación es llevar a un segundo nivel los estudios realizados a nivel laboratorio, el cual consistirá en hacer uso de residuos de BOV expuestos directamente en agua residual de curtiembre, empleando un sistema RBS aerobio como medio de remoción del cromo (VI). Además, se espera que la utilización de la BOV no represente un aumento de DQO y SST al final del tratamiento.
2.1 Colecta y caracterización del agua residual de curtiembre
El agua residual usada para el desarrollo de esta investigación fue colectada específicamente del punto de descarga de la etapa de curtido de una empresa de curtiembre, ubicada en el distrito de Ate, Lima, Perú, con coordenadas geográficas S 12°1´38.02” y E 76°53´39.46”. Su colecta se efectuó tomando como referencia lo descrito por APHA 1985 (citado por Borda, 2016), en recipientes de polietileno de 20 L, que previamente fueron lavados con ácido nítrico (HNO3) y purgados mediante limpiezas sucesivas con la misma agua residual.
Se tomaron muestras del agua residual para obtener los valores de caracterización de los parámetros en estudio (cromo (VI), DQO, SST, pH, temperatura). El manejo de las muestras y la determinación de sus valores se describen en el inciso 2.7 y los resultados se muestran en el Cuadro 1.
2.2 Pretratamiento del agua residual de curtiembre
El pretratamiento del agua residual de curtiembre se llevó a cabo tomando como referencia lo descrito por CONAGUA (2015), se utilizó una rejilla fina de 6.3 mm de apertura para la eliminación de sólidos suspendidos. Luego, se acondicionó con una solución de bicarbonato de sodio (NaHCO₃) hasta alcanzar un pH de 6.8, con la finalidad de preparar el medio para un buen desarrollo del conjunto microbiano (Elahi et al., 2019; Karthik et al., 2017). Finalmente, se tomó muestras del agua residual pretratada, con el objetivo de tener los valores de inicio de los parámetros evaluados (Cuadro 1).
Cuadro 1. Resultados de la caracterización y pretratamiento de los parámetros del agua residual de curtiembre.
Table 1. Results of the characterization and pretreatment of tannery wastewater parameters.
|
Parámetros |
Caracterización |
Pretratamiento |
|
cromo (VI) (mg/L) |
0.660 |
0.494 |
|
DQO (mg/L) |
6 672 |
6 593 |
|
SST (mg/L) |
468 |
334 |
|
pH |
4.88 |
6.80 |
|
Temperatura (°C) |
20.4 |
20.4 |
La BOV fue obtenida a partir de los residuos de poda de los jardines de la municipalidad de Ate, Lima, Perú; específicamente, para la investigación, se usó la Stenotaphrum secundatum.
Como etapa previa a su fragmentación, la BOV fue seleccionada y sometida a lavados sucesivos con agua potable, hasta eliminar todo residuo ajeno a esta. Su fragmentación y tamizado se realizó tomando como referencia lo reportado por Bayarsaikhan et al. (2016); fue fragmentada mecánicamente (mortero de porcelana + agua destilada) y cribada con un tamiz de 850 μm. Posteriormente, se evaporó el agua por calor (mechero bunsen), para obtener la BOV en polvo. Como paso final, fue esterilizada en autoclave a 121 °C, a 15 psi, durante 30 minutos, y puesta en refrigeración a 4 °C hasta su posterior uso. Cabe resaltar que la concentración de BOV integrada al sistema RBS+BOV fue de 1.5 g BOV/L, con una modificación respecto a lo usado por Gu et al. (2003).
2.4 Obtención de las baterías reductoras de cromo (VI) [BRCrVI]
2.4.1 Aumento bacteriano del agua residual de curtiembre
Se inoculó 1 mL de muestra tomada del agua residual de curtiembre en 100 mL de medio LB Lennox - Sigma Aldrich (Triptona 10 g/L, extracto de levadura 5 g/L, NaCl 5 g/L) que previamente fue esterilizada en autoclave a 121 °C, a 15 psi, durante 15 minutos. Luego se incubó a 30 °C, durante 48 horas.
2.4.2 Selección o aislamiento de las BRCrVI
Esta etapa fue desarrollada tomando como referencia lo empleado por Ramírez et al. (2013). Se diluyó 1.6 g de dicromato de potasio (K2Cr2O7) –CDH en 200 ml de agua destilada; de esta forma, se obtuvo la disolución madre de K2Cr2O7 a 8 000 ppm. Después se prepararon diluciones seriadas a partir de la solución madre, para obtener concentraciones de K2Cr2O7 a 8 000 ppm, 4 000 ppm, 2 000 ppm y 1 000 ppm. A cada una de estas 4 disoluciones se le agregó 4 g de medio LB Miller - Himedia (Triptona 10 g/L, agar 15 g/L, extracto de levadura 5 g/L, NaCl 5 g/L), para posteriormente llevar a autoclave a 121 °C, a 15 psi, durante 15 minutos. Se dejó enfriar hasta alcanzar una temperatura de 45 °C y se plaqueó, independientemente, en 4 placas Petri.
La selección o aislamiento de las BRCrVI se realizó empleando la técnica de siembra de microorganismo por estrías, a partir del resultado que se obtuvo en la etapa de aumento bacteriano del agua residual de curtiembre. Luego se llevaron a incubación a 31 °C, durante 48 horas.
Finalmente, se seleccionó la placa Petri; 8 000 ppm, donde se evidenció un crecimiento bacteriano con mayor resistencia al K2Cr2O7. Dicha placa fue usada para la etapa de aumento de las BRCrVI.
En un volumen de 3 000 mL de agua destilada, se agregó 60 g de medio LB Lennox - Sigma Aldrich y se esterilizó en autoclave a 121 °C, a 15 psi, durante 15 minutos. Después de alcanzar una temperatura de 45 °C, se integró las colonias de las BRCrVI de la placa Petri de 8 000 ppm y se llevaron a incubación a 31 °C, durante 48 horas.
Las BRCrVI se obtuvieron de conformidad con lo empleado por Zhao et al. (2012). Estas fueron centrifugadas a 6 000 rpm, a 4 °C, por 5 minutos. Del volumen total de 3 000 mL del aumento, se obtuvo 60.3 g de BRCrVI. Finalmente, las BRCrVI fueron integradas a los sistemas RBS2 y RBS+BOV a una concentración de biomasa microbiana de 0.6 g/ L.
Para determinar el tipo de bacteria, se hizo uso de un microscopio óptico (NIKON, E100-LED) y se empleó la técnica de tinción de Gram. El resultado evidenció un bacilo Gram negativo aerobio.
2.5 Diseño y operatividad del RBS aerobio
Las características de diseño del sistema RBS aerobio se definieron con base en lo descrito por Cárdenas et al. (2006), como se presenta en la Figura 1. El RBS aerobio consistió en un recipiente cilíndrico de polietileno de 0.28 m de diámetro, con una altura de 0.33 m y un volumen total de 20 L. Cabe resaltar que el diseño del RBS aerobio fue de aplicación para todos los sistemas descritos en el Cuadro 2.
Cada RBS aerobio fue llenado con agua residual de curtiembre a un volumen de reacción de 18 L, acoplado a un mecanismo de aireación por un mini compresor (RESUM, ACO-0084), el cual inyectó aire a razón de 12.7 L/min. Además, este empleó agitación mecánica cada 15 min, durante 5 segundos y operando a una temperatura ambiente inicial de 22.2 °C (Figura 1).
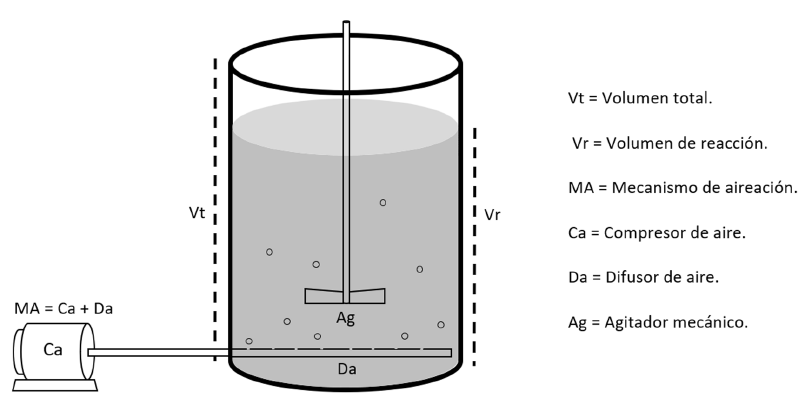
Figura 1. Características de diseño del RBS aerobio.
Figure 1. Design features of the aerobic RBS.
2.6 Diseño y operatividad de la parte experimental
Se implementaron 2 sistemas controles (RBS1 y RBS2) y otro de estudio (RBS+BOV). Cada uno estuvo conformado por un total de 3 réplicas por sistema, con los siguientes elementos descritos en el Cuadro 2.
El arranque de los sistemas dio inicio luego de integrar lo colocado en el Cuadro 2. Se evaluó los parámetros de cromo (VI), pH y temperatura, durante los tiempos de 12 h, 24 h y 36 h de operación de los sistemas. La DQO y SST se determinó al inicio y al final de operación de los sistemas (36 h). Se estableció un intervalo de reposo de 5 horas de los sistemas para la toma de las muestras.
Cuadro 2. Resumen de cómo está conformada la parte experimental.
Table 2. Summary of how the experimental part is made up.
|
Sistemas |
Réplicas |
Componentes de los sistemas |
|
RBS1 |
3 |
ARC*(18 L), aireación (12,5 L) |
|
RBS2 |
3 |
ARC*(18 L), aireación (12,5 L), BRCrVI (0.6 g/L) |
|
RBS+BOV |
3 |
ARC*(18 L), aireación (12,5 L), BRCrVI (0.6 g/L), BOV (1.5 g/L) |
* ARC: agua residual de curtiembre.
2.7 Determinación de cromo (VI), DQO, SST, pH y temperatura
Las muestras para cromo (VI) fueron colectadas en envases de polietileno de 500 ml y su conservación se efectuó adicionando NaOH hasta alcanzar un pH de 9.4. La determinación de cromo (VI) se hizo de acuerdo con el método 218.5 de la EPA (1982) y su cuantificación fue por espectrometría de absorción atómica de llama (APHA et al., 2017a), empleando un espectrofotómetro de absorción atómica (marca Thermo scientific, modelo ICE-3500).
Las muestras para la DQO fueron almacenados en envases de polietileno de 100 ml y su conservación se realizó adicionando H2SO4 hasta alcanzar un pH < 2. La determinación de la DQO fue mediante el método 5220D (método de reflujo cerrado) (APHA et al., 2017b), utilizando un reactor digital (marca Hach, modelo DRB-200).
Los SST se analizaron por el método 2540D (sólidos totales en suspensión secados a 103-105 °C) (APHA et al., 2017c), con una estufa de calor (marca Memmert, modelo UF110).
La determinación de pH y temperatura se obtuvo con un multiparámetro digital (marca Hanna, modelo HI98129).
La normalidad de los datos se determinó mediante la prueba Shapiro Wilk, con un nivel de significancia p > 0.05. El análisis de varianza se obtuvo por ANOVA, con un nivel de significancia p < 0.05, seguido de una prueba de Tukey a posteriori, con un nivel de significancia p < 0.05. Todas se realizaron mediante el programa SPSS statistics y se aplicaron a todos los parámetros en estudio.
2.9 Determinación de porcentajes de remoción
Los porcentajes de remoción de cromo (VI) se determinaron utilizando la Ecuación 1 (Shang et al., 2017). Esta también fue adaptada para establecer los porcentajes de remoción de DQO y SST.
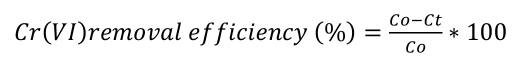 (E.1)
(E.1)
Donde: Co: concentración inicial de cromo (VI) en mg/L.
Ct: concentración de cromo (VI) en un tiempo “x” en mg/L.
Los porcentajes de remoción del cromo (VI) por los sistemas se muestran en la Figura 2. De los 3 sistemas, el RBS+BOV presentó un mayor porcentaje de remoción de cromo (VI) en los 3 periodos de operación (12 h = 86.4 %, 24 h = 91.5 %, 36 h = 93 %). Se atribuye estos resultados a sus componentes (BOV y BRCrVI), es decir, a su capacidad para eliminar el cromo (VI) de forma independiente y a la combinación de ambos. Estudios han determinado que la biomasa orgánica vegetal (BOV) posee grupos funcionales y radicales libres responsables de la remoción y reducción del cromo (VI), por medio de mecanismos de adsorción, complejación y biotransformación química (Scaglia et al., 2013; Yaashikaa et al., 2019; Zhang et al., 2017). Por otra parte, los resultados obtenidos por Selvakumar et al. (2021) y Thatoi et al. (2014) concluyeron que los microrganismos o BRCrVI tienen la capacidad de remover el cromo (VI) por mecanismos de reducción bioquímica y complejación química, ya que estos cuentan con un tipo de enzima (cromato reductasa) localizada en fracciones solubles en su citoplasma o en su membrana celular, la cual cataliza la reducción del cromo (VI) a estados oxidativos más estables. Por último, el trabajo de Tacher et al. (2015) a escala laboratorio ha evidenciado que los ácidos húmicos de la materia orgánica natural (MON) mejoran la capacidad de la bacteria Shewanella oneidensis para eliminar cromo (VI), ya que los AH promueven la reacción redox extracelular de ella y mejoran tanto su actividad microbiana como su consecuente eliminación de cromo (VI). Cabe resaltar que, a la fecha, los resultados del presente estudio no pueden ser comparados, pues no se ha encontrado indagación alguna que replique aplicar BOV para remover cromo (VI) de una muestra real de agua residual de curtiembre dentro de un RBS aerobio como medio de eliminación. Los casos que se referencian en este trabajo simulan el agua residual de curtiembre con soluciones acuosas sintéticas de cromo (VI).
En lo que respecta al sistema SBR2, mostró porcentajes de remoción de cromo (VI) menores a los valores obtenidos por el sistema RBS+BOV, pero superior al RBS1, con valores que van desde 63.2 % = 12 h, 71.5 % = 24 h, 80.1 % = 36 h. Estos resultados se atribuyen a su principal componente, es decir, a la capacidad de las BRCrVI para biodegradar y eliminar el cromo (VI), por los mecanismos descritos en el párrafo superior (Selvakumar et al., 2021; Thatoi et al., 2014).
Por último, el sistema RBS1 presenta los menores porcentajes de remoción de cromo (VI), con valores que van desde 0.2 % = 12 h, 0.6 % = 24 h, 2.6 % = 36 h. Este resultado no sorprende, ya que dicho sistema no contó con componente alguno (BOV y BRCrVI) que permita la remoción de cromo (VI) de forma directa o en combinación. Sin embargo, se asume que los valores mínimos de remoción obtenidos se deben, básicamente, al efecto reductor del agua residual de curtiembre, es decir, a la presencia de bacterias autóctonas en el agua residual en estudio, que posibilitaron disminuir la concentración del cromo (VI) durante el tiempo en el cual el sistema operaba.
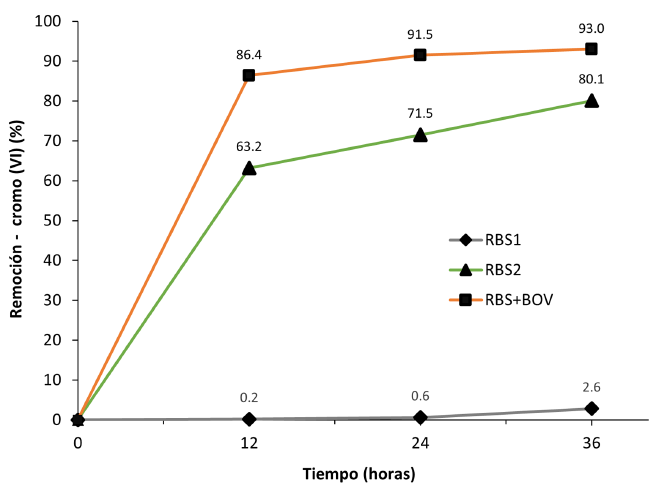
Figura 2. Remoción de cromo (VI) por los sistemas, en los 3 periodos de operación.
Figure 2. Removal of chromium (VI) by the systems, in the 3 operating periods.
Por otro lado, se observó que el comportamiento de los porcentajes de remoción de cromo (VI), durante los periodos de operación, muestran una tendencia de crecimiento exponencial, con excepción del RBS1 (Figura 2). Ello sugiere que dicho comportamiento estaría determinado por efecto directo del crecimiento exponencial de las BRCrVI. Cabe resaltar que el RBS2 y RBS+BOV, a diferencia del RBS1, tuvieron como componente a las BRCrVI. En los resultados de Ramírez et al. (2013), se reportó que a concentraciones de cromo (VI) consideradas tolerables para las bacterias que biodegradan este contaminante se evidenció que los porcentajes de remoción de cromo (VI) estuvieron determinados por el crecimiento exponencial bacteriano. Esto explicaría, igualmente, por qué para los tiempos de 24 h y 36 h se ve una disminución de los porcentajes de remoción de cromo (VI), debido a que las BRCrVI estarían finalizando la fase exponencial e ingresando a la estacionaria, fase en la cual se nota un descenso del crecimiento microbiano, por efecto de la disminución de nutrientes en el sistema.
Los valores de DQO se midieron al inicio, después de incorporar la BOV al sistema RBS+BOV y al final del tratamiento (36 h). La prueba estadística Tukey arrojó que no hubo diferencia significativa en las concentraciones y los porcentajes de remoción de la DQO en los sistemas RBS+BOV y RBS2 al término del tratamiento. Estos alcanzaron de 767 a 807 mg/L y 87.8 a 88.4 %, superiores a los obtenidos por el RBS1 (5 099 mg/L y 22.7 %). Esto lleva a concluir que la BOV no participa en eliminar DQO y que los componentes propios de un sistema RBS (aireación y las BRCrVI) fueron los responsables directos. Estudios como los de Durai et al. (2011), Malakahmad et al. (2011) y Wei et al. (2012) reportaron que los componentes propios de un sistema RBS aerobio (aireación y BRCrVI) eliminaron la DQO por mecanismos de oxidación y biodegradación de la materia orgánica en porcentajes mayores a 70 %, similares a los obtenidos en el presente trabajo. Por otro lado, el sistema RBS1 presentó un porcentaje de remoción de DQO considerable, atribuyendo este resultado a su único componente (aireación) y a su capacidad para oxidar la materia orgánica.
Cuadro 3. Remoción de DQO por los sistemas, expresada en mg/L, y porcentaje de remoción.
Table 3. COD removal by the systems, expressed in mg/L, and removal percentage.
|
Sistemas |
DQO inicio (mg/L) |
DQO al incorporar BOV (mg/L) |
DQO final (mg/L) |
DQO final (%) |
|
RBS1 |
6 593 |
5 099 |
22.7 |
|
|
RBS2 |
6 593 |
807 |
87.8 |
|
|
RBS+BOV |
6 593 |
6 727 |
767 |
88.4 |
Por otro lado, se ha logrado evidenciar que la BOV incorporada al sistema RBS+BOV, no provoca un aumento de la DQO al final del tratamiento, y que esta terminó precipitando por efecto del tiempo de reposo establecido (5h) para los sistemas. Lo expuesto se muestra en el Cuadro 4, donde se puede apreciar que el peso del precipitado del sistema RBS+BOV es superior a los obtenidos por RBS1 y RBS2, y que la diferencia de peso no es más que la BOV precipitada, la cual se integró postinicio del arranque de los sistemas.
Cuadro 4. Peso seco de los precipitados obtenidos al final del tratamiento.
Table 4. Dry weight of the precipitates obtained at the end of the treatment.
|
Sistemas |
BOV incorporado al sistema al inicio del tratamiento (g) |
Precipitados al final del tratamiento (g) |
|
RBS1 |
38.7 |
|
|
RBS2 |
39.1 |
|
|
RBS+BOV |
27 |
66.8 |
Los cambios de pH en RBS2 y RBS+BOV aumentaron a medida que transcurría el tiempo de tratamiento, con excepción de RBS1, donde los cambios no fueron significativos (Figura 3). Por otro lado, la prueba estadística (Tukey) arrojó que no hubo diferencia significativa en el aumento de pH entre RBS2 y RBS+BOV, pues estos tuvieron un mismo comportamiento. Los resultados muestran que la BOV no participa en los cambios de pH en los sistemas y que las BRCrVI fueron las responsables de ellos. Dicho hallazgo es contrastado con lo descrito por Panigatti et al. (2012), quienes evidenciaron que el aumento de pH de un medio se atribuye al crecimiento bacteriano. Las bacterias, a medida que biodegradan los sustratos presentes del medio, forman en el proceso compuestos alcalinos, en consecuencia, aumentan el pH del medio.
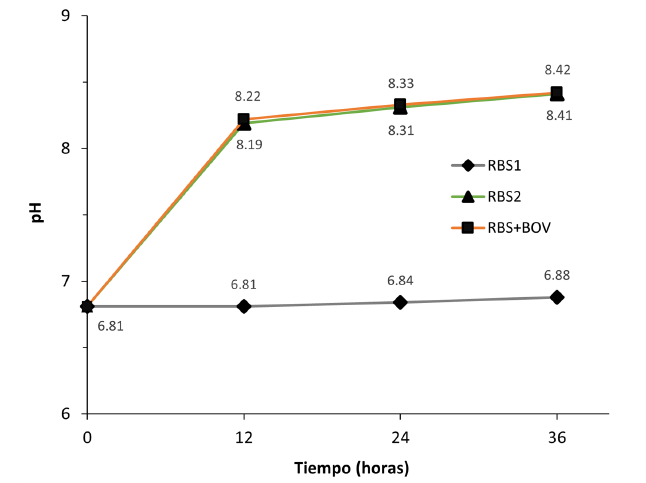
Figura 3. Cambio del pH de los sistemas en el tiempo, atribuido al efecto directo de las BRCrVI.
Figure 3. Change in the pH of the systems over time, attributed to the direct effect of BRCrVI.
3.4 Concentración de cromo (VI) en función del pH
Se constató que, a medida que aumentaba el pH de los sistemas RBS1 y RBS+BOV, los porcentajes de remoción de cromo (VI) también crecían, con excepción del RBS1 que no mostró acrecentamiento alguno (Figura 4). A partir de ello, se ha observado que existe una relación directamente proporcional entre el incremento del pH y los porcentajes de remoción de cromo (VI). Otros estudios han demostrado que el aumento de los porcentajes de remoción de cromo (VI), por efecto de los AH de la BOV, se efectúan con mayor eficacia a medida que los valores de pH bajan; se llega a valores óptimos de remoción que oscilan entre 2 y 3.5 (Rambabu et al., 2020; Yaashikaa et al., 2019; Zhang et al., 2017). Los resultados de estos hallazgos contradecirían los obtenidos en la Figura 4. Sin embargo, Gu et al. (2003) evidenciaron que, cuando el pH del medio aumenta a valores cercanos a neutro o ligeramente alcalino, las fracciones de AH de la BOV facilitan la remoción del cromo (VI) de las BRCrVI (S. putrefaciens CN32). Según Tacher et al. (2015), los AH de la BOV promueven la reacción redox extracelular de la BRCrVI, así que mejoran su actividad microbiana y, consecuentemente, la eliminación de cromo (VI) a medida que aumenta el pH del medio a valores que oscilan entre 6 y 9 (Elahi et al., 2019; Karthik et al., 2017; Sarankumar et al., 2020). Además, Panigatti et al. (2012) atribuyen la elevación de pH de un medio al metabolismo bacteriano. Esto demuestra que el aumento de los porcentajes de remoción de cromo (VI), a medida que aumenta el pH, se atribuye directamente a la BRCrVI y a la mediación de la BOV, en el metabolismo de estas.
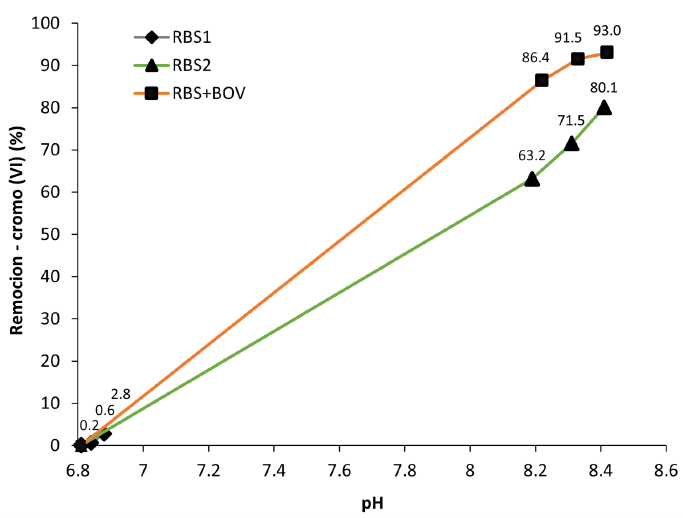
Figura 4. Aumento de los porcentajes de remoción de cromo (VI), relacionados con el incremento de pH de los sistemas.
Figure 4. Increase in chromium (VI) removal percentages, related to the increase in pH of the systems.
Los SST fueron evaluados al inicio, después de haber integrado la BOV al sistema RBS+BOV y al final del tratamiento (36 h). La prueba estadística (Tukey) dio como resultado que no hubo diferencia significativa de los SST obtenidos al concluir dicho tratamiento en los 3 sistemas (RBS1, RBS2, RBS+BOV). Sin embargo, todos presentaron porcentajes de remoción considerables (Cuadro 5). Este resultado sugiere que los componentes de los sistemas (aireación, BRCrVI y BOV) no tuvieron efecto alguno en la remoción de los SST y que la eliminación de este parámetro dependió, en su totalidad, del tiempo de reposo establecido para los sistemas (5 h). Además, se ha podido evidenciar que la BOV incorporada en el RBS+BOV postinicio del arranque de los sistemas no ha afectado, en lo absoluto, en un aumento de los SST al término del tratamiento. Esto se puede apreciar en el Cuadro 5, donde todos los valores de SST para los 3 sistemas no difieren estadísticamente uno del otro.
Cuadro 5. Remoción de SST por los sistemas, expresada en mg/L, y porcentaje de remoción.
Table 5. TSS removal by the systems, expressed in mg/L, and removal percentage.
|
Sistemas |
SST inicio (mg/L) |
SST al incorporar BOV (mg/L) |
SST final (mg/L) |
SST final (%) |
|
RBS1 |
334 |
121 |
63.8 |
|
|
RBS2 |
334 |
110 |
67.1 |
|
|
RBS+BOV |
334 |
887 |
103 |
69.2 |
En lo que respecta al comportamiento de las temperaturas de RBS1, RBS2 y RBS+BOV, el análisis estadístico (Tukey) arrojó que no hubo diferencia significativa de dicho parámetro en los 3 periodos de operación, pues estos tuvieron un mismo comportamiento (Cuadro 6). Por otro lado, los estudios han demostrado que la temperatura influye, en gran medida, en la actividad metabólica de las BRCrVI, así que estas tienen una mayor capacidad para reducir el cromo (VI) en medios donde aquella es superior a 30 °C (Elahi et al., 2019; Karthik et al., 2017; Sarankumar et al., 2020; Zhao et al., 2012). En cuanto a los estudios en los cuales se evaluó la capacidad de la BOV para remover cromo (VI), se ha establecido que la temperatura no es un factor determinante que influya en la capacidad de remoción del cromo (VI) por la BOV. Se han reportado porcentajes considerables de remoción de cromo (VI) a temperatura ambiente, que oscilan entre 20 y 30 °C (Rambabu et al., 2020; Tacher et al., 2015; Zhang et al., 2017), similares a los obtenidos en el presente trabajo. Sin embargo, el panorama lleva a considerar la posibilidad de alcanzar un mayor porcentaje de remoción de cromo (VI) en esta investigación, si se acondicionara el medio del RBS a temperaturas superiores a los 30 °C.
Cuadro 6. Resultados de temperatura durante los periodos evaluados, que estadísticamente no difieren uno del otro.
Table 6. Temperature results during the evaluated periods, which statistically do not differ from each other.
|
Sistemas |
Temperatura (°C) |
|||
|
Inicio |
12 h |
24 h |
36 h |
|
|
RBS1 |
22.2 |
23.2 |
22.3 |
23.3 |
|
RBS2 |
22.2 |
23.4 |
22.4 |
23.4 |
|
RBS+BOV |
22.2 |
23.5 |
22.6 |
23.6 |
Los resultados obtenidos en la presente investigación evidencian la capacidad de la BOV para remover cromo (VI) de un efluente residual de curtiembre en un 93 % de eficiencia. Esto garantiza la viabilidad del aprovechamiento de BOV, con el afán de mitigar los efectos derivados de la inadecuada gestión de las aguas residuales de curtiembre y de los desechos sólidos orgánicos. Además, se respalda la compatibilidad de la BOV con el sistema RBS aerobio, como medio adecuado para la remoción de cromo (VI) del agua residual de curtiembre.
La concentración de los parámetros de cromo (VI) = 0.66 mg/L, DQO = 6672 mg/L, SST = 468 mg/L y pH = 4.88 del agua residual de curtiembre, durante su caracterización, resultaron estar fuera de los valores máximos admisibles (VMA) y de los límites máximos permisibles (LMP) para la descarga de efluentes a las alcantarillas o aguas superficiales de la industria de curtiembre en el Perú. Lo anterior es un claro ejemplo de la contaminación que representarían las aguas residuales de la industria de curtiembre si fueran vertidos a las alcantarillas o, en algunos casos, a los ríos, sin ningún tratamiento. Por otro lado, al término del tratamiento del agua residual de curtiembre con la BOV, se obtuvieron valores aceptables de cromo (VI) = 0.035 mg/L, DQO = 767 mg/L, SST = 103 mg/L, pH = 8.42 y T = 23.6 °C, en referencia a los VMA y los LMP para la descarga de efluentes de la industria de curtiembre a las alcantarillas o aguas superficiales, con excepción de los SST, para el último caso.
El sistema RBS+BOV obtuvo el mayor porcentaje de remoción de cromo (VI) (93 %), seguido del RBS2 (80.1 %) y RBS1 (2.6 %). Ello implica que la BOV tiene una participación removedora de cromo (VI), de forma independiente: 12.9 % y 90.4 %, si se compara con los otros 2 sistemas.
Se determina que la BOV no participa en la eliminación de la DQO; asimismo, que los componentes propios de un sistema RBS aerobio remueven la DQO, por mecanismo de oxidación de la materia orgánica (aireación) y por el metabolismo de los microorganismos (BRCrVI).
En lo que concierne al aumento del pH de los sistemas compuestos con BRCrVI, este último fue el responsable de generar dichos cambios. Por otro lado, se observó que existe una relación directamente proporcional entre el aumento de pH de los sistemas (RBS2 y RBS+BOV) con el incremento de los porcentajes de remoción de cromo (VI). Se concluye que las BRCrVI también fueron las responsables de generar dicha relación, pero, para este caso en particular, con la mediación de la BOV al mejorar su metabolismo.
La prueba estadística (Tukey) dio como resultado que no hubo diferencia significativa de los SST obtenidos al final del tratamiento para los 3 sistemas (RBS1, RBS2, RBS+BOV). Ello significa que los componentes de esos sistemas (aireación, BRCrVI y BOV) no tienen efecto alguno en la remoción de los SST y que la eliminación de este parámetro depende, en su totalidad, del tiempo de reposo establecido (5 h).
Con respecto al posible escenario del aumento de la DQO y SST, por uso de la BOV durante el tratamiento, se evidenció que este termina precipitando en su totalidad por efecto directo del tiempo de reposo del sistema (5 h). Consecuentemente, el uso de la BOV no representa riesgo alguno de aumento de la DQO o SST, al final del tratamiento.
El análisis estadístico Tukey arrojó que no hubo diferencia significativa de la temperatura en los 3 periodos de operación de los sistemas (RBS1, RBS2 y RBS+BOV). Los estudios mediante los cuales se evaluó la aplicabilidad de la BOV en la remoción de cromo (VI) concluyeron que la temperatura no es un factor influyente en la eliminación de este parámetro. Por otro lado, los trabajos con los que se evaluó el uso de las BRCrVI para la eliminación de cromo (VI) ultimaron que las BRCrVI alcanzan una mayor capacidad de remoción con temperaturas mayores a 30 °C. Ello implica considerar la posibilidad de un aumento en los porcentajes de remoción del cromo (VI) de la presente investigación, si se acondicionara el RBS aerobio a una temperatura igual o superior a los 30 °C.
Por último, se ha podido contrastar las conclusiones de la literatura respecto a la participación de las BRCrVI en la remoción del cromo (VI) y la DQO. Además, su uso en el RBS aerobio lo convierte en parte fundamental de este sistema.
A la Escuela de Ciencias Ambientales de la Universidad Científica del Sur y a quienes aportaron en la revisión del presente trabajo investigativo.
6. Ética y conflicto de intereses
La persona autora declara que ha cumplido totalmente con los requisitos éticos y legales pertinentes, tanto durante el estudio como en la producción del manuscrito; que no hay conflictos de intereses de ningún tipo; que todas las fuentes financieras se mencionan completa y claramente en la sección de agradecimientos; y que está totalmente de acuerdo con la versión final editada del artículo.
7. Declaración de la disponibilidad de datos
Los datos que respaldan los resultados de este estudio serán puestos a disposición por el autor correspondiente, previa solicitud razonable.
Alam, N., Mia, M., Ahmad, F. & Rahman, M. (2020). An overview of chromium removal techniques from tannery effluent. Applied Water Science, 10(9). https://doi.org/10.1007/s13201-020-01286-0
APHA, AWWA & WEF. (2017a). Part. 3111B Direct. Air-Acetylene Flame Method. Standard Methods for the Examination Water and Wastewater. Washington DC.
APHA, AWWA & WEF. (2017b). Method 5220D, Chemical Oxygen Demand. Standard Methods for the Examination Water and Wastewater. Washington DC.
APHA, AWWA & WEF. (2017c). Method 2540D, Total suspended solids dried at 103-105 °C. Standard Methods for the Examination Water and Wastewater. Washington DC.
Bayarsaikhan, U., Ruhl, A. & Jekel, M. (2016). Characterization and quantification of dissolved organic carbon releases from suspended and sedimented leaf fragments and of residual particulate organic matter. Science of the Total Environment, 571, 269-274. https://doi.org/10.1016/j.scitotenv.2016.07.148
Bayuo, J. (2021). An extensive review on chromium (vi) removal using natural and agricultural wastes materials as alternative biosorbents. Journal of Environmental Health Science and Engineering, 19(1), 1193-1207. https://doi.org/10.1007/s40201-021-00641-w
Borda, O. (2016). Evaluación y reducción de los niveles de cromo en muestras de aguas residuales provenientes de curtiembres. L´estrit Ingénieux, 5, 6-12. http://revistas.ustatunja.edu.co/index.php/lingenieux/article/view/1230
Cárdenas, C., Perruolo, T., Tarre, Y., Flores, K., Trujillo, A., Saules, L., Araujo, I. & Yobroudi, S. (2006). Remoción de nutrientes en un reactor discontinuo secuencial. Interciencia, 31(11), 787-793. https://www.redalyc.org/articulo.oa?id=33912206
Castillo, M. & López, J. (2018). Tratamiento del agua residual industrial de la curtiembre Rolemt, para el cumplimiento de los Valores Máximos Admisibles. [Tesis para optar el título de profesional en Ingeniería Ambiental y Prevención de Riesgos, Universidad Privada Antonio Guillermo Urrelo]. Repositorio institucional. http://repositorio.upagu.edu.pe/handle/UPAGU/825
Chen, S. Y., Huang, S., Chiang, P., Kuan, W., Huang, J., Hung, J., Tzou, Y., Chen, C. & Wang, M. (2011). Influence of chemical compositions and molecular weights of humic acids on Cr (VI) photo-reduction. Journal of Hazardous Materials, 197, 337-344. https://doi.org/10.1016/j.jhazmat.2011.09.091
CONAGUA. (2015). Manual de Agua Potable, Alcantarillado y Saneamiento: Diseño de Plantas de Tratamiento de Aguas Residuales Municipales: Pretratamiento y Tratamiento Primario. México: 626. ISBN: 978-607-626-016-6.
Córdova, H., Vargas, R., Cesare, C., Flores, L. & Visitación, L. (2014). Tratamiento de las aguas residuales del proceso de curtido tradicional y alternativo que utiliza acomplejantes de cromo. Revista de la Sociedad Química del Perú, 80(3), 183-191. https://doi.org/10.37761/rsqp.v80i3.226
Cortes, B. & Martínez, S. (2017). Gestión Ambiental Empresarial en el sector de cuero en Bogotá como estrategia competitiva para ingresar al mercado europeo. [Tesis para optar por el título de profesional en Negocios Internacionales, Universitaria Agustiniana]. Repositorio institucional. http://repositorio.uniagustiniana.edu.co/handle/123456789/285
Durai, G., Rajasimmam, M. & Rajamohan, N. (2011). Kinetic studies on biodegradation of tannery wastewater in a sequential batch bioreactor. Journal of Biotech Research, 3, 19-26. http://btsjournals.com/assets/2011v3p19-26.pdf
Elahi, A., Ajaz, M., Rehman, A., Vuilleumier, S., Khan, Z. & Hussain, S. (2019). Isolation, characterization, and multiple heavy metal-resistant and hexavalent chromium-reducing Microbacterium testaceum B-HS2 from tannery effluent. Journal of King Saud University - Science, 31(4), 1437-1444. https://doi.org/10.1016/j.jksus.2019.02.007
EPA, (1982). Chromium, Dissolved hexavalent (Atomic Absoption, furnace Technique) - Method: 218.5. Washington, DC.
Farabegoli, G., Carucci, A., Majone, M., & Rolle, E. (2004). Biological treatment of tannery wastewater in the presence of chromium. Journal of Environmental Management. 71(4), 345-349. https://doi.org/10.1016/j.jenvman.2004.03.011
Ferreira, D., Flores, M., de Olivera, B., Moreira, J., Quintão, T., de Lima, A. & Malafaia, G. (2018). Insights about the toxic effects of tannery effluent on Lithobates catesbeianus tadpoles. Science of The Total Environment, 621(2018), 791-801. https://doi.org/10.1016/j.scitotenv.2017.11.310
Gu, B., & Chen, J. (2003). Enhanced microbial reduction of Cr (VI) and U (VI) by different natural organic matter fractions. Geochimica et Cosmochimica Acta. 67(19), 3575-3582. https://doi.org/10.1016/S0016-7037(03)00162-5
Huiman, A. (2022). Los residuos peligrosos generados en la industria textil peruana para el caso de la Alta costura, fibra de alpaca y curtiembre. Revista del Instituto de Investigación de la Facultad de Minas, Metalurgia y Ciencias Geográficas, 25(49), 115-133. https://doi.org/10.15381/iigeo.v25i49.21097
Jobby, R., Jha, P., Yadav, K. & Desai, N. (2018). Biosorption and biotransformation of hexavalent chromium [Cr(VI)]: A comprehensive review. Chemosphere, 207, 255-266. https://doi.org/10.1016/j.chemosphere.2018.05.050
Kalidhasan, S., Santhana, A., Rajesh, V. & Rajesh, N. (2016). The journey traversed in the remediation of hexavalent chromium and the road ahead toward greener alternatives a perspective. Coordination Chemistry Reviews, 317, 157-166. https://doi.org/10.1016/j.ccr.2016.03.004
Karthik, C., Barathi, S., Pugazhendhi, A., Ramkumar, V., Bao, N. & Indra, T. (2017). Evaluation of Cr (VI) reduction mechanism and removal by Cellulosimicrobium funkei strain AR8, a novel haloalkaliphilic bacterium. Journal of Hazardous Materials, 333, 42-53. https://doi.org/10.1016/j.jhazmat.2017.03.037
Kerur, S., Bandekar, S., Hanagadakar, M., Nandi, S., Ratnamala, G. & Hegde, P. (2021). Removal of hexavalent Chromium Industry treated water and Wastewater: A review. Materials Today: Proceedings, 42, 1112-1121. https://doi.org/10.1016/j.matpr.2020.12.492
Kimbrought, D., Cohen, Y., Winer, A., Creelman, L. & Mabuni, C. (2010). A Critical Assessment of Chromium in the Environment. Critical Reviews in Environmental Science and Technology, 29(1), 1-46. https://doi.org/10.1080/10643389991259164
Kumari, V., Yadav, A., Haq, I., Kumar, S., Naresh, R., Kumar, S. & Raj, A. (2016). Genotoxicity evaluation of tannery effluent treated with newly isolated hexavalent chromium reducing Bacillus cereus. Journal of Environmental Management, 183(1), 204-211. https://doi.org/10.1016/j.jenvman.2016.08.017
Malakahmad, A., Hasani, A., Eisakhani, M. & Isa, M. (2011). Sequencing Batch Reactor (SBR) for the removal of Hg2+ and Cd2+ from synthetic petrochemical factory wastewater. Journal of Hazardous Materials, 191(1-3), 118-125. https://doi.org/10.1016/j.jhazmat.2011.04.045
Monroy, E., Echevarria, M. & Gómez, D. (2021). Diseño y validación de un sistema de adsorción de cromo hexavalente en efluentes de curtiembre usando cáscara de naranja y salvado de trigo. Tecnología y Ciencias del Agua, 12(3), 1-31. https://doi.org/10.24850/j-tyca-2021-03-01
Muñiz, J. (2016). Eficiencia del biosorbente de coronta de maíz para la adsorción del Cromo Hexavalente en aguas residuales de la industria Curtiembre Huachipa - 2016. [Tesis para obtener el título profesional de Ingeniero Ambiental, Universidad César Vallejo]. Repositorio institucional. https://hdl.handle.net/20.500.12692/4668
Najarro, R. (2021). Proceso de adsorción natural con quitosano para la remoción de cromo hexavalente en aguas residuales de curtiembre del segundo tramo del río Huaycoloro, Lima - 2021. [Tesis para optar por el título profesional de Ingeniero Ambiental, Universidad César Vallejo]. Repositorio institucional. https://hdl.handle.net/20.500.12692/74514
Narayanasamy, S., Sundaram, V., Sundaram, T. & Dai-Viet, N. (2022). Biosorptive ascendency of plant based biosorbents in removing hexavalent chromium from aqueous solutions - Insights into isotherm and kinetic studies. Environmental Research, 210. https://doi.org/10.1016/j.envres.2022.112902
Panigatti, M., Torres, J., Griffa, C., Boglione, R., Gentinetta, F. & Cassina, D. (2012). Uso de Escherichia coli para biorremediación de efluente contaminado con cromo (VI). Avances en ciencias e ingeniería, 3(2), 11-24. https://www.redalyc.org/pdf/3236/323627686002.pdf
Rambabu, K., Bharat, G., Banat, F. & Loke, P. (2020). Biosorption performance of date palm empty fruit bunch wastes for toxic hexavalent chromium removal. Environmental Research, 187. https://doi.org/10.1016/j.envres.2020.109694
Ramírez, A. & Benítez, A. (2013). Tolerancia y reducción de cromo (VI) por Bacillus cereus B1, aislado de aguas residuales de una curtiembre. Revista ciencia R, 17(02), 51-63. http://hdl.handle.net/10893/8808
Sánchez, D. (2018). Gestión de riesgo de desastres de las lagunas de oxidación de Covicorti, el Cortijo y propuesta para tratamiento de aguas residuales industriales de curtiembres en la ciudad de Trujillo y distritos. La Libertad. [Tesis para obtener el título profesional de Ingeniero Civil, Universidad Privada Antenor Orrego]. Repositorio institucional. https://hdl.handle.net/20.500.12759/4170
Sánchez, S. (2022). Aplicación de pseudomonas como agente biorreductor del cromo hexavalente de los efluentes de las curtiembres del distrito el Porvenir, 2022. [Tesis para obtener el título profesional en Ingeniería Ambiental, Universidad Privada del Norte]. Repositorio institucional. https://hdl.handle.net/11537/33292
Sarankumar, R., Arulprakash, A., Devanesan, S., Selvi, A., Al Saldi, M., Rajasekar, A. & Ahamed, A. (2020). Bioreduction of hexavalent chromium by chromium resistant alkalophilic bacteria isolated from tannery effluent. Journal of King Saud University - Science, 32(3) 1969-1977. https://doi.org/10.1016/j.jksus.2020.02.010
Saxena, G., Kishor, R., Bharagava, R., Das, P., Gupta, P. & Kumar, G. (2021). Chapter 18 - Emerging green technologies for biological treatment of leather tannery chemicals and wastewate. Bioremediation for Environmental Sustainability, 435-457. https://doi.org/10.1016/B978-0-12-820524-2.00018-3
Scaglia, B., Tambone, F. & Adani, F. (2013). Cr (VI) reduction capability of humic acid extracted from the organic component of municipal solid waste. Journal of Environmental Sciences, 25(3), 487-494. https://doi.org/10.1016/S1001-0742(12)60078-3
Selvakumar, P., Subramanian, D., Natarajan, J. & Ramatchandirane, S. (2021). Analysis of Chromate Transporters in Bacterial Species for Cr(VI) Reduction Isolated from Tannery Effluent Contaminated Site of Dindigul District, Tamil Nadu, India. Geomicrobiology Journal, 38(7), 598-606. https://doi.org/10.1080/01490451.2021.1906359
Shang, J., Zong, M., Yu, Y., Kong, X., Du, Q. & Liao, Q. (2017). Removal of chromium (VI) from water using nanoscale zerovalent iron particles supported on herb-residue biochar. Journal of Environmental Management, 197, 331-337. https://doi.org/10.1016/j.jenvman.2017.03.085
Singh, M. & Srivastava, R. (2010). Sequencing batch reactor technology for biological wastewater treatment: a review. Asia Pacific Journal of Chemical Engineering, 6, 3-13. https://doi.org/10.1002/apj.490
Singh, P. & Chowdhuri, D. (2017). Environmental Presence of Hexavalent but Not Trivalent Chromium Causes Neurotoxicity in Exposed Drosophila melanogaster. Molecular Neurobiology, 54, 3368-3387. https://doi.org/10.1007/s12035-016-9909-z
Solís, C. (2020). Estrategias basadas en producción más limpia y biorremediación para mitigar los impactos ambientales negativos generados por los efluentes industriales de las curtiembres del Parque Industrial de Río Seco, Arequipa. [Tesis para obtener el grado académico de Maestra en Ciencias: Ingeniería de Proyectos, con mención en Gerencia de Exportaciones, Universidad Nacional de San Agustín de Arequipa]. Repositorio institucional. https://repositorio.unsa.edu.pe/server/api/core/bitstreams/1f73fdb1-a5d9-4652-b6d9-cf8a94af462a/content
Tacher, R., Hsu, L., Ravindra, V., Nealson, K. & Pirbazari, M. (2015). Modeling the transport and bioreduction of hexavalent chromium in aquifers: Influence of natural organic matter. Chemical Engineering Science, 138, 552-565. https://doi.org/10.1016/j.ces.2015.08.011
Thatoi, H., Das, S., Mishra, J., Rath, B. & Das, N. (2014). Bacterial chromate reductase, a potential enzyme for bioremediation of hexavalent chromium: A review. Journal of Environmental Management, 146, 383-399. https://doi.org/10.1016/j.jenvman.2014.07.014
Wei, Y., Ji, M., Li, R. & Qin, F. (2012). Organic and nitrogen removal from landfill leachate in aerobic granular sludge sequencing batch reactors. Waste Management, 32(3), 448-455. https://doi.org/10.1016/j.wasman.2011.10.008
Yaashikaa, P. R., Senthil Kumar, P., Mohan Babu, V. P., Kanaka Durga, R., Manivasagan, V., Saranya, K. & Saravanan, A. (2019). Modelling on the removal of Cr(VI) ions from aquatic system using mixed biosorbent (Pseudomonas stutzeri and acid treated Banyan tree bark). Journal of Molecular Liquids, 276, 362-370. https://doi.org/10.1016/j.molliq.2018.12.004
Zhang, J., Chen, L., Yin, H., Jin, S., Liu, F. & Chen, H. (2017). Mechanism study of humic acid functional groups for Cr (VI) retention: Two-dimensional FTIR and 13C CP/MAS NMR correlation spectroscopic analysis. Environmental Pollution, 225, 86-92. https://doi.org/10.1016/j.envpol.2017.03.047
Zhao, C., Yang, Q., Chen, W., & Teng, B. (2012). Removal of hexavalent chromium in tannery wastewater by Bacillus cereus. Canadian Journal of Microbiology. 58, 23-28. https://doi.org/10.1139/w11-096
1 Ingeniero ambiental, egresado de la Universidad Científica del Sur, Lima, Perú. camacllanqui.h@gmail.com; https://orcid.org/0000-0001-7158-2595
Escuela de Ciencias Ambientales,
Universidad Nacional, Campus Omar Dengo
Apartado postal: 86-3000. Heredia, Costa Rica
Teléfono: +506 2277-3688
Correo electrónico revista.ambientales@una.ac.cr



